缓冲溶液可以抵抗少量酸或碱对溶液PH的影响。人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系(H2CO3/HCO3-),以维持血液PH的稳定。已知人体正常体温时,H2CO3 HCO3-+H+的Ka=10-6.1,正常血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3,lg5=0.7则下列判断正确的是
HCO3-+H+的Ka=10-6.1,正常血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3,lg5=0.7则下列判断正确的是
| A.正常人血液内Kw=10-14 |
| B.由题给数据可算得正常人血液的pH约为7.4 |
| C.正常人血液中存在:c(HCO3-)+c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) |
| D.当过量的碱进入血液中时,只发生反应:HCO3-+OH—=CO32-+H2O |
马格尼特法冶炼镁的工艺流程如下图。炉料中除有煅烧白云石和硅铁外,还加入煅烧过的铝土矿,加Al2O3的主要目的是降低渣的熔点,便于液态排渣。
已知白云石的成分为CaCO3·MgCO3,硅铁是指含有55%硅左右的铁[可表示为Si(Fe)],作还原剂,最后得到低品位的硅铁[可表示为Fe(Si)],简易流程图如下
试回答下列问题
(1)反应①,白云石煅烧得CaO·MgO的化学方程式为:。
(2)反应②,还原炉中发生反应生成镁和炉渣的化学方程式为:。
(3)该成分的沪渣是一种工业生产的重要原料,可作为生产原料。
(4)马格尼特法冶炼镁,一台4500千瓦的炉子可日产约7.2吨镁,一天至少约消耗含硅60%的硅铁吨。
已知A、E、I、L是常见的非金属单质,其中A为淡黄色固体,Z是常见的金属单质,B的相对分子质量比A大32,C的相对分子质量比B大16,Y是一种常见的液体,J是磁铁矿的主要成分,D、H、K均是重要的工业产品,X分子的球棍模型如图所示,图中部分反应条件已略去。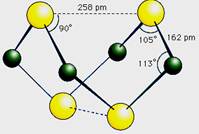
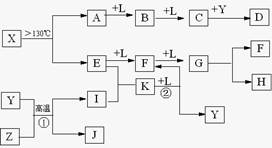
试回答下列问题
(1)写出化学式:DX 。
(2)E的电子式为:。
(3)写出化学方程式:①;②。
X、Y、Z三种元素的原子,核外均未出现3d电子。已知:1、 X+和Y-两种离子具有相同的核外电子排布类型;2、 Z元素原子核内的质子数比Y元素原子核内的质子数少9。 请回答下列问题:
(1)写出X、Y、Z三种元素的元素符号X,Y, Z。
(2)Y元素能形成多种含氧酸,其中酸性最强的含氧酸的化学式为 。
(3)含有这三种元素的一种化合物常在实验室中用来制备O2,写出该反应的化学方程式: 。每生成1molO2,转移的电子数为 mol。
A~H以及X、Y的转化关系如图: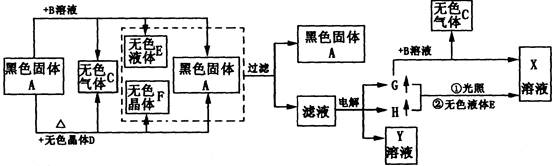
(1)电解上述滤液时产生G的电极是。其电极反应式为。
(2)取上图中滤液做焰色反应显紫色,上图中焰色反应显紫色的还有。
(3)写出黑色固体与X浓溶液共热反应的离子方程式。
(4)写出G与B溶液反应的化方程式。
有X、Y、Z、W四种短周期元素,原子序数依次增大。X的阳离子就是一个质子。Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体。Y原子的最外层电子数是次外层电子数的2倍。请回答:
(1)Z2的电子式为,Y的原子结构示意图为,YW2的结构式为。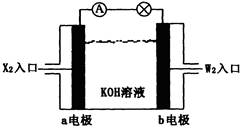
(2)将X2、W2按上图所示通入某燃料电池中,其中,b电极的电极反应式为。若有16gW2参加反应,转移的电子数是NA。
(3)由X、Y、Z、W四种元素组成的无机酸酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为。