一定温度下,将CI2缓缓通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,溶液PH变化的曲线如图所示。则下列叙述中正确的是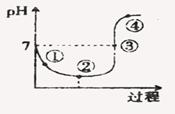
| A.点①所示溶液中c(H+) =c(C l-)+c(HClO)+c(OH-) |
| B.点②所示溶液中:c(H+)>c(Cl-)>c(ClO-)>c(HClO) |
| C.点③所示溶液中:c(Na+)=2c(ClO-)+c(HClO) |
| D.点④所示溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(HClO) |
设NA为阿伏加德罗常数,下列叙述正确的是
| A.常温常压下,22.4 L NO2中含有NA个分子 |
| B.1 mol羟基中电子数为10 NA |
C.R2+的质量数为A,中子数为N,则n g R该价态的氧化物中含质子数为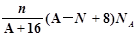 |
| D.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA |
下列说法正确的是
| A.232Th 转换成233U是化学变化,233U和235U的化学性质几乎相同 |
| B.防止自行车钢架生锈主要是利用了电化学防腐原理 |
| C.血液透析是利用了胶体的聚沉性质 |
| D.葡萄酒中含有的微量的二氧化硫具有抗氧化剂作用 |
25°C时,c(CH3COOH)+c(CH3COO-)=0.1mol/L的醋酸、醋酸钠混合溶液中,c(CH3COOH)、
c(CH3COO-)与pH的关系如图所示。下列有关该溶液的叙述不正确的是
| A.pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.溶液中:c(H+)+c(Na+)=c(CH3COO-)+c(OH-) |
| C.由W点可以求出25°C时CH3COOH的电离常数 |
| D.pH=4的溶液中:c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1mol/L |
将10.7 g Mg、Al和Fe组成的合金溶于足量的氢氧化钠溶液中,产生标准状况下3.36 L气体。另取等质量的合金溶于过量盐酸中,生成标准状况下7.84 L气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀物质的量为
| A.0.1 mol | B.0.2 mol | C.0.25 mol | D.0.3 mol |
下列离子方程式正确的是
| A.以金属银为阳极电解饱和NaCl溶液:2Cl-+2H2O =H2↑+Cl2↑+2OH- |
| B.FeBr2溶液中通入足量的氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| C.硫酸亚铁溶液中加入用硫酸酸化的双氧水Fe2++2H++H2O2=Fe3++2H2O |
| D.在通入过量SO2后的NaOH溶液中加足量的溴水(不考虑SO2的溶解):HSO3-+Br2+H2O=3H++2Br-+SO42- |