在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是
| A.滴加石蕊试液显红色的溶液 Fe3+、NH4+、Cl-、SCN- |
| B.pH值为1的溶液 Cu2+、Na+、Mg2+、NO3- |
| C.水电离出来的c(H+)=10-13mol/L的溶液 K+、HCO3-、Br-、Ba2+ |
| D.所含溶质为Na2SO4的溶液 K+、CO32-、NO3-、Al3+ |
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如下所示,下列说法正确的是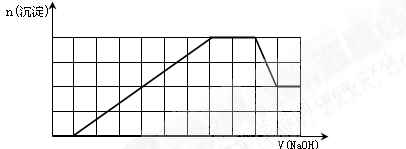
| A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+ |
| B.原溶液中一定含有SO42-和Na+ |
| C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 |
| D.反应最后形成的溶液中含有的溶质为Na2SO4 |
对溶液中的离子进行鉴定,下列实验所得结论不合理的是()
| A.向溶液中加入稀硝酸后,再加入AgNO3溶液有白色沉淀生成,则溶液中可能含有Cl- |
| B.向溶液中加入KSCN溶液,观察无明显现象,继续加入氯水,溶液变红色,说明溶液中一定含有Fe3+ |
| C.向溶液中加入NaOH溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推测该溶液中含有NH4+ |
| D.向溶液中加入盐酸,产生使澄清石灰水变浑浊的无色无味气体,可推测溶液中含有CO32- |
下图表示可逆反应A(s)+B(g) nC(g);ΔH=Q(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述中一定正确的是( )
nC(g);ΔH=Q(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述中一定正确的是( )
| A.其他条件相同,a表示使用了催化剂,b没有使用催化剂 |
| B.其他条件相同,若只改变温度,则a比b的温度高且ΔH>0 |
| C.其他条件相同,若只改变压强,则a比b的压强大且n≥2 |
| D.其他条件相同,若改变A的物质的量,则a比b消耗A的物质的量少 |
NA为阿伏加德罗常数,下列叙述中正确的是 ()
| A.0.1 mol PCl3中形成共价键的电子数是0.3NA |
| B.100 mL 1 mol/L NaHSO4溶液中HSO4—数是0.1NA |
| C.标准状况下,11.2 L CO2和O3混合气体中含有的原子数是1.5 NA |
| D.17 g H2O2完全分解,转移电子数是1NA |
下列化学反应的离子方程式正确的是()
| A.次氯酸钠漂液中加浓盐酸产生氯气:ClO- + Cl-+2H+=Cl2↑+H2O |
| B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C.用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S↑ |
| D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-=CaSO4↓+H2O |