在一固定容积的密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L,0.1 mol/L,0.2 mol/L, 当反应达到平衡时,可能存在的数据是
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L,0.1 mol/L,0.2 mol/L, 当反应达到平衡时,可能存在的数据是
| A.SO2为0.4 mol/L,O2为 0.2 mol/L | B.SO2为0.25 mol/L |
| C.SO2、SO3均为0.15 mol/L | D.SO3为0.4 mol/L |
NA表示阿伏加德罗常数.下列说法中正确的是( )
| A.Cu和足量的稀硝酸反应产生4.48L气体时,转移的电子数为0.6NA |
| B.1.2g NaHSO4晶体中阳离子和阴离子的总数为0.03 NA |
| C.标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA |
| D.S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期, Z、M同主族;X+与M2—具有相同的电子层结构;离子半径:Z2—>W—;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是
| A.X、M两种元素只能形成X2M型化合物 |
| B.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| C.元素Y、Z、W的单质晶体属于同种类型的晶体 |
| D.元素W和M的某些单质可作为水处理中的消毒剂 |
已知下列热化学方程式,则③中的Q3值为
Zn(s)+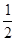 O2(g)=ZnO (s)△H=" -" Q1 kJ• mol-1①
O2(g)=ZnO (s)△H=" -" Q1 kJ• mol-1①
Hg(l) +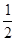 O2(g)=HgO (s)△H= -Q2 kJ• mol-1②
O2(g)=HgO (s)△H= -Q2 kJ• mol-1②
Zn(s) +HgO (s) =Hg(l)+ ZnO (s)△H= -Q3 kJ• mol-1③
| A.Q2 -Q1 | B.Q1 +Q2 | C.Q1- Q2 | D.-Q1- Q2 |
X、Y、M、Z四种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素。下列说法不正确的是
| A.化合物YZ3极易溶解于水 |
| B.Z与M可以形成含有非极性键的化合物 |
| C.12 g14X中含有中子的物质的量为8 mol |
| D.由上述四种元素组成的离子化合物受热易分解 |
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图3中每个“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是 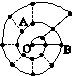
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族
C.B元素是图中金属性最强的元素
D.A、B组成的化合物中可能含有共价键