已知:A是石油裂解主要产物之一,其产量常用于衡量一个石油化工发展水平的标志。E是一种具有香味的液体乙酸乙酯,下列是有机物之间的转化关系:
(1)A、E的结构简式分别为__________________、____________________。
(2)A→B的反应类型为________________________。
(3)C所含的官能团名称_______________,鉴定它可用的试剂为____________。
(4)写出B→C的化学反应方程式:________________________。
(5)在实验室我们也可以用图所示的装置制取乙酸乙酯。其中饱和碳酸钠溶液的主要作用是_______________________________ 。
(6)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防_____________________________ 。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是__
_____。
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应).某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究.
Ⅰ.铁矿石中含氧量的测定
①按如图组装仪器, ;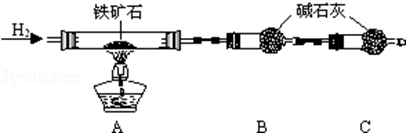
②将10.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却.
(1)补全步骤①的操作 .
(2)装置C的作用为 .
(3)测得反应后装置B增重2.7g,则铁矿石中氧的质量百分含量为 .
Ⅱ.
(1)步骤④中煮沸的作用是 .
(2)下列有关步骤⑥的操作中说法正确的是 .
a.滴定管用蒸馏水洗涤后可以直接装液
b.锥形瓶不需要用待测液润洗
c.滴定过程中,眼睛注视滴定管中液面变化
d.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(3)若滴定过程中消耗0.5000mol•L﹣1的KI溶液25.0mL,则铁矿石中铁的质量百分含量为 .
某课外活动小组用如图装置进行实验,试回答下列问题。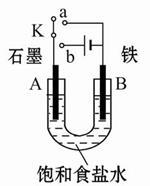
(1)若开始时开关K与a连接,则B极的电极反应式为 。
(2)若开始时开关K与b连接,则B极的电极反应式为 ,
总反应的离子方程式为 。
有关上述(2)实验,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。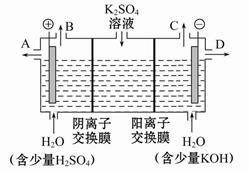
①该电解槽的阳极反应式为 。
此时通过阴离子交换膜的离子数 (填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
②若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为 。
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供艇员呼吸之用,它与二氧化碳反应的化学方程式为2Na2O2+2CO2===2Na2CO3+O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95克过氧化钠样品为原料,制取O2,设计出如下实验装置:
(1)A中制取CO2的装置,应为下列图①、②、③中的图________________。
B装置的作用是_ 。为了检验E中收集到的气体,在取出集气瓶后, 。
(2)若E中的石灰水出现轻微白色浑浊,请说明原因:________________。
(3)反应完毕时,若测得E中的集气瓶收集到的气体为250 mL,又知氧气的密度为1.43 g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值__________(填“大”或“小”),相差约________mL(取整数值,所用数据均在标准状况下测定),这是由于__________________________。
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。
CO(NH2) 2+ 2NaOH + NaClO = Na2CO3 + N2H4·H2O + NaCl
实验一: 制备NaClO溶液
(1)将氯气通入到盛有NaOH的锥形瓶中,锥形瓶中发生反应的离子方程式是_______________;
实验二: 制取水合肼(实验装置如图所示)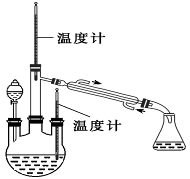
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充 分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(已知:N2H4·H2O + 2NaClO = N2↑ + 3H2O + 2NaCl)
(2)分液漏斗中的溶液是 (填标号A或B);
A.NaOH和NaClO混合溶液
B.CO (NH2) 2溶液
选择的理由是 ;
实验三: 测定馏分中肼含量
水合肼具有还原性,可以生成氮气。测定水合肼的质量分数可采用下列步骤:
a.称取馏分5.000g,加入适量NaHCO3固体,经稀释、转移、定容等步骤,配制250mL溶液。
b.移取25.00 mL于锥形瓶中,加入10mL水,摇匀.
c.用0.2000mol/L碘溶液滴定至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右。记录消耗碘的标准液的体积。
d.进一步操作与数据处理
(3)水合肼与碘溶液反应的化学方程式 ;滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是
(4)滴定时,碘的标准溶液盛放在 滴定管中(选填:“酸式”或“碱式”) ;若本次滴定消耗碘的标准溶液为18.00mL,馏分中水合肼(N2H4·H2O)的质量分数
为 (保留三位有效数字);
(5)为获得更可靠的滴定结果,步骤d中进一步操作主要是: 。
实验室有一包固体粉末样品可能是MgCO3、Fe2O3和FeO的混合物。
I.甲学生设计实验方案,以确定样品中是否含有FeO。除样品外,实验室只提供以下试剂:KMnO4溶液、盐酸、稀硫酸、KSCN溶液、NaOH溶液,请你描述甲学生的实验操作步骤、现象及结论: 。
Ⅱ.经甲学生实验确定该样品中不存在FeO,乙学生想在甲学生的实验基础上进一步来测定混合物中Fe2O3的含量:乙学生准备用如图所示各仪器按一定顺序连接成一套完整的装置进行实验,以测定Fe2O3的质量分数。
请回答下列问题:
(1)盛装盐酸的仪器的名称是 ,装置的连接顺序是:_____→_____→______→_____(填图中字母序号,各仪器只能选用一次)。
(2)实验过程中需要持续通入空气,其作用除可以起到“搅拌”A、D中反应物以实现充分反应外,还有一个重要作用是:____________________________。
(3)为提高测定的准确度,在B中最应加入的物质是: (填字母编号)。
a.饱和NaHCO3溶液 b.蒸馏水 c.浓硫酸 d.NaOH溶液
(4)在进行乙学生的实验方案评价时,有学生认为不必测定A中沉淀的质量,而只要测出装置A在吸收反应产生的气体前后的质量差,就能完成实验要求。实验证明,若用此法测得Fe2O3的质量分数将__________(填“偏大”、“偏小”或“不变”)。