把V L含有MgS04和K2S04的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
| A.mol·L-1 | B.mol·L-1 |
| C.mol·L-1 | D.mol·L-1 |
某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )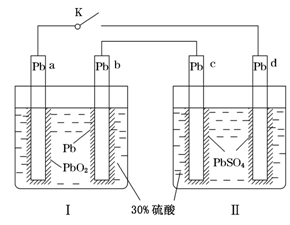
| A.闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42— |
| B.当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol |
| C.闭合K时,Ⅱ中SO42—向c电极迁移 |
| D.闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极 |
下列液体均处于25℃,有关叙述正确的是
| A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
| C.AgCl在同浓度的CaCl2,和NaCI溶液中的溶解度相同 |
| D.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)> C(CH3COO-) |
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为: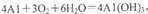 ,下列说法不正确的是
,下列说法不正确的是
A.正极反应式为: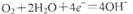 |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需更换铝板就可继续使用 |
现有等浓度的下列溶液:①醋酸,②次氯酸,③碳酸氢钠,④碳酸,⑤碳酸钠。按溶液pH由小到大排列正确的是
| A.④①②⑤③ | B.④①②③⑤ |
| C.①④②③⑤ | D.①④②⑤③ |
下列离子能大量共存的是