用下列实验装置进行的实验中,不能达到相应实验目的的是 ( )
| A.装置甲:防止铁钉生锈 | B.装置乙:萃取碘水中的碘 |
| C.装置丙:实验室制取乙酸乙酯 | D.装置丁:海水蒸馏得淡水 |
下列热化学方程式正确的是(注:ΔH的绝对值均正确)( )
| A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-1 367.0 kJ·mol-1(燃烧热) |
| B.Ba(OH)2(aq)+2HCl(aq)===BaCl2(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1(中和热) |
| C.S(s)+O2(g)===SO2(g) ΔH=-269.8 kJ·mol-1(反应热) |
| D.2NO2===O2+2NO ΔH=+116.2 kJ·mol-1(反应热) |
一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料说法正确的是
| A.在熔融电解质中,O2-由负极移向正极 |
| B.电池的总反应是:2C4H10 + 13O2 → 8CO2 + 10H2O |
| C.通入空气的一极是正极,电极反应为:O2 + 4e- 2H2O= 4OH- |
| D.通入丁烷的一极是正极,电极反应为:C4H10 + 26e- + 13O2 = 4CO2 + 5H2O |
反应aA(g)+bB(g) cC(g)+dD(g)改变条件达到平衡后D的浓度随条件改变的关系如下图,试判断此反应的系数关系和△H正负()
cC(g)+dD(g)改变条件达到平衡后D的浓度随条件改变的关系如下图,试判断此反应的系数关系和△H正负()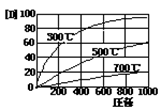
| A.a+b<c+d,△H<0 | B.a+b<c+d,△H>0 |
| C.a+b>c+d,△H<0 | D.a+b>c+d,△H>0 |
下列推论正确的是( )
| A.S(g)+O2(g)===SO2(g) ΔH=a;S(s)+O2(g)===SO2(g) ΔH=b;则a>b |
| B.C(石墨,s)===C(金刚石,s) ΔH=+1.9 kJ/mol,则可判定石墨比金刚石稳定 |
| C.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.4 kJ/mol,则含20 g NaOH的溶液与稀盐酸完全反应,放出的热量为28.7 kJ |
| D.CaCO3(s)===CaO(s)+CO2(g) ΔH>0,则该反应任何温度下都能自发进行 |
已知H2(g)+I2(g) 2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
| A.甲、乙提高相同温度 | B.甲中加入0.1mol He,乙不变 |
| C.甲降低温度,乙不变 | D.甲增加0.1mol H2,乙增加0.1mol I2 |