(6分)(1)下列实验设计或操作合理的是__________。
a.实验室制溴苯时选用的试剂可以是溴水、苯和铁屑。
b.配制银氨溶液时,将氨水逐滴加到 AgNO3溶液中,边加边振荡,直至沉淀恰好完全消失。
c.将10滴溴乙烷加入到1mL10%的烧碱溶液中,加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子。
d.实验室制乙炔时,为了减慢反应速率,可用饱和食盐水代替蒸馏水。
(2)溴水是中学化学实验中常用的一种试剂,用溴水可鉴别出下列各组物质,试写出发生反应的化学方程式。
①苯酚与乙醇
②乙烯与乙烷
有5瓶白色固体试剂,分别是氯化钡、氢氧化钠、硫酸钠、硫酸铵、无水硫酸铜,现只提供蒸馏水,通过下面的实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体试剂分别加入5支试和中,加入适量蒸馏水,振荡试管,观察到的现象是
被检出的物质的化学式是
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式是:
1支试管中有白色沉淀生成(书写离子方程式)
1支试管中有蓝色沉生成(书写离子方程式)则被检出的物质的化学式是和;
(3)鉴别余下未检出物质的方法和观察到的现象是:
写出发生反应的化学方程式。
已知有以下物质相互转化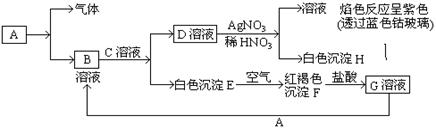
试回答:(1)写出B的化学式。
(2)写出由E转变成F的化学方程式。
(3)写出用KSCN鉴别G溶液的离子方程式
化合物A(C8H17Br)经NaOH醇溶液处理后生成两种烯烃B1和B2。B2(C8H16)经过:①用臭氧处理;②在Zn存在下水解,只生成一种化合物C。C经催化氢化吸收1 mol氢气生成醇D(C4H10O),用浓硫酸处理D只生成一种无侧链的烯烃E(C4H8)。已知:(注:R1、R3可为H或其他烃基)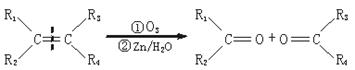
试根据已知信息写出下列物质的结构简式:
A;B2
C ______ ___ __;E_______.
《宋史·食货志》中有这样一段话:“浸铜之法,以生铁煅成薄铁片,排置胆水槽中,浸渍数日,铁片为胆水所薄,上生赤煤。去刮赤煤,入炉三炼成铜。大率用铁二斤四两得铜一斤。”
(1)文中胆水可能是赤煤又可能是
(2)上文中炼铜,假如生铁中含铁95%,那么铁的利用率是
(1斤以16两计算)
某研究性学习小组在实验室合成了一种物质A。
⑴经分析,A的相对分子质量不超过100,A中C、H的质量分数分别为:w(C)=69.76%,w(H)=11.63%,且完全燃烧后产物只有CO2和H2O。则A的摩尔质量为_________。
⑵ A的核磁共振氢谱如下图所示,且A可以和金属钠反应生成H2,但不能在Cu作催化剂下被催化氧化。(提示:羟基与碳碳双键相连的结构不稳定)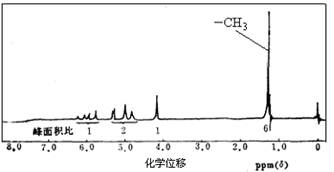
(3)请根据以上信息写出A的结构简式。
(4)A的某种同分异构体B分子中不含支链,能发生银镜反应。写出B发生银镜反应的化学方程式_______________。