下列操作或者说法错误的是
| A.除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯 |
| B.除去苯中的少量苯酚:加入NaOH溶液,振荡、静置分层后,除去水层 |
| C.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
| D.提取溶解在水中的少量碘:加入CCl4,振荡、静置分层后,取出有机层再分离 |
下列说法中,正确的是
| A.在纸上层析操作时,要让试样点刚好接触展开剂,否则不能很好地分离。 |
| B.实验室制备硝基苯时,先将浓硫酸滴入浓硝酸后,冷却,再边振荡边滴加苯。 |
| C.从海带中提取碘的方法是:取样→灼烧→溶解→过滤→萃取。 |
| D.向盛有少量Na2O2的试管中加入少量水,并立即滴入2滴酚酞,振荡,溶液呈红色。 |
已知热化学方程式N2(g) + 3H2(g)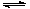 2NH3(g) + Q kJ(Q>0),下列说法中,正确的是
2NH3(g) + Q kJ(Q>0),下列说法中,正确的是
| A.1mol N2(g)和3mol H2(g)具有的能量之和低于2 mol NH3(g)具有的能量 |
| B.将1mol N2 (g)和3mol H2 (g)置于一密闭容器中充分反应后放出Q kJ的热量 |
| C.升高温度,平衡向逆反应方向移动,上述热化学方程式中的Q值减小 |
| D.将一定量N2(g)和H2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有3mol H2被氧化 |
设NA为阿伏加德罗常数的值。下列叙述中,正确的是
| A.12.0gNaHSO4晶体中阳离子和阴离子的总数为0.3 NA |
| B.14g分子式CnH2n的链烃中含有的碳碳双键的数目一定为NA/n |
| C.标准状况下,1L液态水中含有的H+数目为10-7NA |
| D.足量Zn与一定量的浓硫酸反应,产生22.4L气体时,转移的电子数为2 NA |
下列说法中,正确的是
| A.35Cl、37 Cl为互为同位素,有不同的化学性质 |
| B.氯气和二氧化硫使品红褪色的原理相同 |
| C.浓硝酸和浓硫酸在空气中放置一段时间后浓度都会降低 |
| D.卤化氢在空气中都能形成白雾,它们都是强电解质 |
针对下图装置的说法中,正确是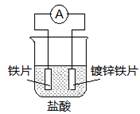
| A.溶液中pH值明显下降 |
| B.铁片为正极,镀锌铁片为负极 |
| C.阴极的电极反应式:Fe-2e→Fe2+ |
| D.电子由锌经溶液流向铁 |