根据图中包含的信息分析,下列叙述正确的是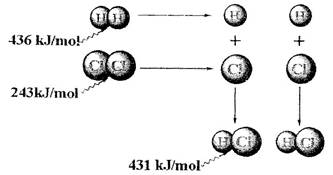
| A.氢气与氯气反应生成1 mol氯化氢气体,反应吸收248 kJ的能量 |
| B.436 kJ/mol是指断开1 mol H2中的H-H键需要放出436 kJ的能量 |
| C.氢气与氯气反应生成2 mol氯化氢气体,反应放出183 kJ的能量 |
| D.431kJ/mol是指生成2 mol HCl中的H-Cl键需要放出431 kJ的能量 |
“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是
| A.非金属单质燃烧时火焰均为无色 |
| B.NaCl与Na2CO3灼烧时火焰颜色相同 |
| C.焰色反应均应透过蓝色钴玻璃观察 |
| D.只有金属单质灼烧时火焰才有颜色 |
下列反应的离子方程式书写正确的是( )
| A.氯化铝溶液中加入过量氨水:Al3+ + 4NH3?H2O |
| B.氧化钠与水反应:O2—+H2O = 2OH- |
| C.碳酸钙溶于醋酸:CaCO3 + 2H+ |
| D.氯化亚铁溶液中通入氯气:2Fe2+ + Cl2 |
下列叙述正确的是()
| A.有氧元素参加的反应一定是氧化还原反应 |
| B.反应前后元素化合价没有变化的反应一定不是氧化还原反应 |
| C.某元素在化学反应中,由化合态变为游离态,则该元素一定被还原 |
| D.氧化还原反应中,一种物质被氧化,另一种物质必被还原 |
据报道,科学家已成功合成了少量的O4,有关O4的说法正确的是
| A.O4的摩尔质量是64 g |
| B.O4与O2互为同位素 |
| C.相同质量的O4与O3所含原子个数之比为1∶1 |
| D.O4与O3、O2都是氧元素的同分异构体 |
下列类型的反应,一定发生电子转移的是
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |