2011年3月11日日本地震损坏核电站设备,引起核泄漏。钚是核工业重要原料,原子核内质子数为94,有多种同位素如钚—238、钚—242、钚—244等,下列关于钚—238说法错误的是
| A.钚是f 区元素 | B.核外电子数238 |
| C.核内中子数 144 | D.钚是锕系元素 |
全钒液流电池是一种新型的绿色环保储能电池,该电池性能优良,其电池总反应为:v3++VO2++H2O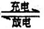 VO2++2H++V2+。下列叙述正确的是
VO2++2H++V2+。下列叙述正确的是
| A.充电时阳极附近溶液的酸性减弱 |
| B.充电时阳极反应式为:VO2++2H++e-=VO2++H2O |
| C.放电过程中电解质溶液中阳离子移向负极 |
| D.放电时每转移1mol电子,负极有1mol V2+被氧化 |
下列各溶液中的离子可能大量共存的是
| A.由水电离的c(OH-)=10-14mol·L-1的溶液:CH3COO-、SO42—、Na+、K+ |
| B.加入铝粉后产生大量氢气的溶液:NH4+、Na+、NO3-、Cl-、SO42- |
| C.能使pH试纸变深蓝色的溶液中: S2一、SO32-、CO32-、Na + |
| D.无色溶液中:K+、Na+、MnO4-、SO42- |
下列除杂所选用的试剂及操作方法均正确的组合是(括号内为杂质)
| 选项 |
待提纯的物质 |
选用的试剂 |
操作方法 |
| A |
I2(H2O) |
CCl4 |
萃取、分液 |
| B |
CO2(CO) |
O2 |
点燃 |
| C |
Zn (Cu) |
稀硫酸 |
过滤 |
| D |
乙醇(水) |
生石灰 |
蒸馏 |
在恒温、恒容下,发生如下反应:2A(g)+2B(g)  C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1 和6 mol·L—1 ,以下叙述正确的是
C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1 和6 mol·L—1 ,以下叙述正确的是
A、达到平衡时,途径I的反应速率等于途径Ⅱ的反应速率
B、达到平衡时,途径I所得混合气体的压强等于途径Ⅱ所得混合气体的压强
C、两途径最终达到平衡时,体系内各组分的百分含量相同
D、两途径最终达到平衡时,体系内各组分的百分含量不相同