在一定温度下有甲、乙两容积相等的密闭容器(两容器容积保持不变)。
(1)向甲容器中通入3 mol N2和4 mol H2,反应达到平衡时,生成NH3amol。此时,NH3的物质的量分数是________。(用含有“a”的表达式表示)。若在达到平衡状态的甲容器中通入少量的N2,则达到新平衡时,体系中N2的体积分数将________(选填“增大”、“减小”或“不变”)。
(2) 若起始时,向乙中通入6mol N2和8mol H2,达到平衡时,生成的NH3的物质的量为b mol, (选填“>”、“<”或“=”)。
如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL,求通电前A池中原混合溶液Cu2+的浓度。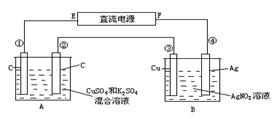
2.22克某元素的氯化物XCl2溶于水形成溶液后,加入40ml 1mol/L AgNO3溶液恰好完全反应。已知该元素原子核内的质子数和中子数相等。
(1)求X元素的质子数和质量数
(2)写出X元素在周期表中的位置
将6.5克锌投入200mL某浓度的盐酸中,锌完全反应,反应前后溶液的体积不变。请用详细的过程,
求:
(1) 反应中生成的H2在标准状况下的体积;
(2) 取反应后的溶液20mL,加入足量的AgNO3溶液,生成白色沉淀5.74克,求原盐酸中HCl的物质的量
浓度。
将一定量由碳、氢、氧三种元素组成的有机化合物A的蒸气与4.8g氧气混合点燃,再将生成的气体依次通过①盛有浓硫酸的洗气瓶②饱和石灰水(设每个装置中的反应物均过量)。经测定①中增重3.60g②中增重8.80g。A蒸气的密度是相同条件下H2的38倍。又测知该有机物既能与碳酸钠溶液反应又能与金属钠反应,且均有气体生成,但得到的气体在相同条件下体积不同。试求该有机物的分子式,并写出其可能的结构简式。
如图为100mL 2 mol /L 的AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。试回答: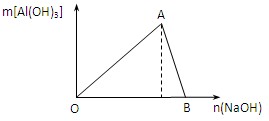
(1) A点时已参加反应的AlCl3和NaOH的物质的量之比为1比。
(2) AB段曲线所表示的反应的离子方程式是___________________。
(3) B处溶液中存在的物质的量浓度最大的离子是(填离子符号)。向B处生成的溶液中通入二氧化碳,可见到的现象是。
(4)如在该AlCl3溶液中生成7.8克沉淀,则消耗的氢氧化钠的物质的量为mol或mol。