某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是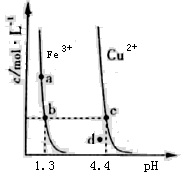
| A.Ksp<Ksp2 |
| B.加适量NH4Cl固体可使溶液由a点变到b点 |
| C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等 |
| D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和 |
2005年3月29日京沪高速淮安段发生一起特大交通事故,一辆载有液氯的铁罐车因轮胎爆炸造成大量液氯泄漏,给当地居民的生活和环境造成严重污染。下列有关说法合理的是()
| A.液氯泄漏将当地大片庄稼熏黄,这是由于Cl2的漂白性所致 |
| B.泄漏的液氯应该用大量碱液中和 |
| C.液氯泄漏后立即挥发成氯气而扩散到空气中,故事故现场不必进行特别的处理 |
| D.这次事故说明液氯不能用铁罐盛装 |
0.5mol氢气和0.5mol碘晶体完全反应,生成1mol碘化氢气体,吸收26.5 kJ 的热,则下列热化学方程式正确的是()
A.H2(g) + I2(s)  2HI(g) - 26.5kJ 2HI(g) - 26.5kJ |
B.H2 + I2 2HI - 53kJ 2HI - 53kJ |
C.H2(g) + I2(s)  2HI(g) - 53kJ 2HI(g) - 53kJ |
D.0.5H2 + 0.5I2  HI - 26.5kJ HI - 26.5kJ |
人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有()
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
砹是原子序数最大的卤族元素,推测砹或砹的化合物最不可能具有的性质是()A
①砹化氢很稳定②砹单质与水反应,使砹全部转化成氢砹酸和次砹酸
③砹是黑色固体④砹化银难溶于水⑤砹易溶于某些有机溶剂
| A.只有①② | B.只有①②⑤ | C.只有③⑤ | D.只有②⑤ |
下列化学式可称为分子式的是()
| A.NaNO3 | B.NH4Cl | C.H2SO4 | D.SiO2 |