(10分)研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。利用反应6NO2+ 8NH3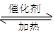 7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH="-196.6" kJ·mol-1
2SO3(g) ΔH="-196.6" kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH="-113.0" kJ·mol-1
2NO2(g) ΔH="-113.0" kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1: 2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= 。
电解原理在化学工业上有广泛应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,
①电解池中X极上的电极反应式为_________________________________,
在X极附近观察到的现象为 。
②Y电极上的电极反应式 ,
检验该电极反应产物的方法是
。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液(说明:杂质发生的电极反应不必写出)
①X电极的材料是________,电极反应式为___________________________ 。
②Y电极的材料是________,电极反应式为______________________________。
常温下有浓度均为0.05mol/L的四种溶液:①Na2CO3②NaHCO3
③HCl ④NH3·H2O,回答相关问题:
(1)上述溶液中,可发生水解的是(填序号)
(2)上述溶液中,既能与NaOH溶液反应,又能与H2SO4溶液反应的溶液中,离子浓度大小的关系
(3)向④中加入少量NH4Cl固体,此时c(NH4+/OH-)的值(“增大”、“减小”或“不变” )
(4)若将③和④的溶液混合后,溶液恰好呈中性,则混合前③的体积④的体积(“大于”、“小于”或“等于” )
(5)取10mL的③溶液,加水稀释到500mL,则此溶液中由水电离出的c(H+)=mol/
(1)实验室在配制氯化铁溶液时,常出现少许浑浊,原因离子方程式表示为 。为防止出现这样的现象,在配制时常加入
(2)根据下列2个热化学反应方程式:
FeO(s)+CO(g)=" Fe(s)+" CO2(g)△H= ―218kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g)△H= +640.5kJ/mol
写出CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学反应方程式:
______________
(4)常温下,等物质的量的浓度的①氨水②NH4HSO4③NH4Cl④(NH4)2CO3
⑤(NH4)2SO4溶液中,c(NH4+)由大到小的顺序为_____________________________(填序号)
在容积为V L的密闭容器中发生2NO22NO+O2的反应。反应过程中NO2的物质的量随时间变化的状况如图所示。
(1)若曲线A和B表示的是该反应在某不同条件下的反应状况,则该不同条件是
A.有、无催化剂 B温度不同C.压强不同
(2)写出该反应的化学平衡常数K的表达式,并比较K800℃K850℃(填>、<或=)。
(3)求 在B条件下从反应开始至达到平衡,氧气的反应速率VO2=。
在B条件下从反应开始至达到平衡,氧气的反应速率VO2=。
(4)不能说明该反应已达到平衡状态的是
A.V正(NO2)=V逆(NO)
B.C(NO2)=C(NO)
C.气体的平均摩尔质量不变
D.气体的密度保持不变
已知
化学反应①:Fe(s)+CO2(g)=FeO(s)+CO(g),其平衡常数为K1;
化学反应②:Fe(s)+H2O(g)=FeO(s)+H2(g),其平衡常数K2。
在温度973 K和1173 K情况下,K1、K2的值分别如下:
| 温度 |
K1 |
K2 |
| 973 K |
1.47 |
2.38 |
| 1173 K |
2.15 |
1.67 |
(1)通常表格中的数值可以推断:反应①是____________(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)=CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=____________。
(3)根据反应①与②可推导出 K1、K2与K3之间的关系式____________。据此关系式及上表数据,也能推断出反应③是____________(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有____________(填写序号)。
K1、K2与K3之间的关系式____________。据此关系式及上表数据,也能推断出反应③是____________(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有____________(填写序号)。
A.缩小反应容器容积 B.扩大反应容器容积 C.降低温度 D.升高温度
E .使用合适的催化剂 F.设法减少CO的浓度
.使用合适的催化剂 F.设法减少CO的浓度