(10分)有A、B、C、D四种离子化合物,组成它们的离子分别为:
阳离子:Na+、Al3+、NH4+; 阴离子:OH-、NO3-、CO32-、HSO4-
为鉴别四种化合物,某学生分别取少量固体配成溶液,编号为A、B、C、D进行实验。实验过程和记录如下图所示(无关物质已略去)

(1) Y、Z的化学式分别为:Y ;Z
(2)写出指定反应的离子方程式:
①加热条件下,C与过量B反应:
②D溶液显弱碱性的原因是(用离子方程式表示)
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是(用化学式表示)
(4)若B、C的稀溶液混合后(不加热)溶液呈中性,则溶液中离子浓度从大到小的顺序是:
A、Z、R、D、E、F、G是七种原子序数依次增大且不大于20的元素,其中有两种非金属元素位于同一土族。己知A、Z、D均能与R形成原子(或离子)个数不同的儿种常见化合物。请回答下列有关问题。
(1)若X、Y是D、F形成的最高价氧化物对应的水化物,浓度均为0.1mol/L的X、Y溶液的pH之和为14,则X、Y的晶体熔点相对高低为(写化学式),导致这种差异存在的原因是在相同温度下,相等物质的量浓度的X、Y各自的溶液中,由水电离出的c(H+)的相对大小关系为。
(2)A与Z、E均可形成正四面体构型的气态分子Q、P,又知P的燃烧热为1430kJ/mol.则其燃烧的热化学方程式。
(3)R与D、F间;R与F、G间均可形成多种化合物,其中有两种是目前广泛使用的具有消毒杀菌能力的化合物。则相同物质的量浓度的这两种物质的溶液,消毒杀菌能力较强的物质的化学式为,另一种物质的溶液中,各离子浓度由大到小的顺序为。
(4)上述七种元素间能形成多种常见二元化合物,其中Z与G形成的一种化合物存在两类化学键的物质溶于HC1溶液的化学反应方程式为,ZR2的电子式是,该分子的空间构型为化合物ZRF2的结构式为____
(5)R能形成多种单质,如R2、R3,研究表明,新近制得的一种组成为R4的分子中,每个R原子均与另外两个R原子各形成一个键,则1molR4中共用电子对数为____NA,列有关R4的说法中正确的是
①R4与R3、R2互为同位素
②R4不能与A、Z、D的单质反应
③R4中各原予最外层均为8电子结构
④R4是1种新型化合物
在氧化还原反应中,氧化过程和还原过程是同时发生的。
Cu2O—2e-+2H+=2Cu2++H2O是一个氧化过程的反应式,下列五种物质FeSO4、Fe2(SO4)2、CuSO4、Na2CO3、KI中的一种能使上述氧化过程顺利发生。
(1)写出并配平该反应的离子方程式:;
反应中氧化剂和还原剂的物质的量之比是。
(2)向(1)中反应后的溶液里,加入酸性高锰酸钾溶液,反应的离子方程式为
;CH2+、MnO4、Fe3+的氧化性由强到弱的顺序是(用离子符号表示)。
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO(g) + 2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
右图是反应I反应过程中的能量变化曲线。
(1)由右图可知反应I为反应(选填”吸热、放热”),反应热△H1=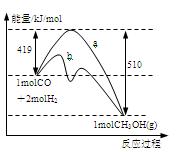
(2)反应I在一定体积的密闭容器中进行,能判断其是否达到化学平衡状态的依据是。
| A.容器中压强不变 | B.混合气体中c(CO)不变 |
| C.v正(H2)=v逆(CH3OH) | D.c(CO)=c(CH3OH) |
(3)图中曲线表示使用催化剂时反应的能量变化。
(4)一定条件下,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数数
K值=(用分数表示),若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡时CH3OH的转化率为,若平衡后在充入4 mol的N2,则C(CO2)是。
(5)从绿色化学的角度比较上述两种方法,符合原子经济的是。(填“I” 或“II”)
现有室温下浓度均为1×10-3mol/L的几种溶液①盐酸、②硫酸、③醋酸、④氯化铵、⑤氨水、⑥NaOH溶液,回答下列问题:
(1)PH均等于3的溶液①、②、③、④中水电离产生的c(H+)的比值是
(2)将③、⑥混合后,若溶液呈中性,则消耗两溶液的体积为③⑥(填“>”、“<”或“=”),溶液中的离子浓度由大到小的顺序为
(3) 将等体积的①、⑤混合,则溶液的PH7(填“>”、“<”或“=”),用离子方程式说明其原因
(4)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的顺序为,最终产生H2总量的关系为
(5)向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,混合液的PH大小关系为①③(填“>”、“<”或“=”)
(6)若将等体积的⑤、⑥溶液加热至相同温度后,溶液的PH⑤⑥(填“>”、“<”或“=”)
X、Y、Z为周期表中常见元素,原子序数递增,X、Y原子的最外层电子数是其电子层数的2倍,Z单质是生产生活中用量最大的金属。
(1)X、Y的原子可构成一种物质,该物质与某能引起温室效应的气体结构相同;该物质的电子式是。
(2)下列含氧酸根离子的化学式书写不正确的是(填序号)。
a.XO3- b.XO32- c.YO32-d.Y2O32- e. YO3- f. YO42-
(3)Z单质与其它化合物可满足如下转化关系:
①C溶液在储存时应加入少量Z,其理由是(用文字和离子方程式回答)________。
②将5~6滴B的饱和溶液滴入沸水中,可得到红褐色液体,该液体能产生丁达尔效应。该反应的离子方程式为。
(4)Y的最高价含氧酸是重要的化工产品。
①已知YO2被空气氧化,每生成1mol气态YO3,放出98.3kJ热量。该反应的热化学方程式是。
②实验测得相同条件下一定量的Y单质分别在空气和在氧气中充分燃烧后产物的成分(体积分数)如下表。
| YO2 |
YO3 |
|
| 空气 |
94%—95% |
5%—6% |
| 氧气 |
97%—98% |
2%—3% |
Y在纯氧中燃烧的产物中YO3含量比在空气中燃烧YO3含量少,试分析其原因。