请根据下图所示的实验过程和提供的数据,试回答下列问题: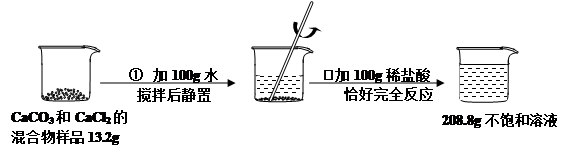
(1)在第②步实验操作中,观察到的一项实验现象是: 。
(2)第①步实验操作后,烧杯中溶液里含有的溶质是(写化学式) 。
(3)计算原混合物样品中CaCl2的质量(写出计算过程,结果精确至0.1g)。
火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式为:
2CaCO3(粉末)+2SO2 + O2 ="==" 2CaSO4+2CO2.
(1)若100克废气中含6.4克二氧化硫,则处理100克这种废气需含碳酸钙(CaCO3)80%的石灰石 克;
(2)处理上述100克废气,可得到含CaSO4 85%的粗产品多少克?(请写出计算过程)
某化工厂利用海水资源进行联合生产,制备氢氧化钠和甲醇等物质。其化工流程如下:
已知:2H2+CO CH3OH
CH3OH
回答下列问题:
(1)电解食盐水的化学方程式为: ;在实验室进行电解水的实验中,为了增强导电性,往往向水中加入少量稀硫酸,而不能加入氯化钠,理由是 。
(2)若该工厂每天可生产80吨甲醇(CH3OH),需要提供 吨氢气。
(3)该工厂每生产80吨甲醇需要消耗多少吨26%的氯化钠溶液?(第3问写出计算过程)
实验室用锌和稀硫酸反应制取氢气的化学方程式为:Zn+H2SO4═ZnSO4+H2↑,要制取0.6克氢气,需要锌多少克?如果反应后所得到的ZnSO4溶液质量为200克,计算所得到的ZnSO4溶液的溶质质量分数是多少?(保留一位小数)
蛋白质是由多种氨基酸[丙氨酸:CH3CH(NH2)COOH等]构成的极为复杂的化合物,人体通过食物获得蛋白质,在胃肠道里与水发生反应,生成氨基酸,试计算:丙氨酸中碳、氢、氧、氮元素的质量比.
鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小刚和小勇同学进行了如下实验。实验过程和测定的相关实验数据如下所示:请回答相关问题:
(1)逸航同学根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;
(2)鑫烁同学根据“反应过程中减少的质量”,也求得了蛋壳中碳酸钙的质量分数,请你写出鑫烁的计算过程和结果。
(3)逸航和鑫烁根据不同的数据求得蛋壳中碳酸钙的质量分数有明显差别,请你分析其中可能的原因 。