某元素A的原子结构示意图为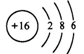
该元素原子的核电荷数为 ,
原子的最外层电子数是 ,A属 元素。(填金属、非金属或稀有气体),A原子通过得失电子而形成的离子的符号是 。
下图为氧化汞受热分解时的微观过程示意图:
根据以上示意图,写出该反应的化学方程式。从图示中我还发现构成物质的粒子有。
按下列要求书写化学方程式:
⑴天然气的主要成分甲烷在空气中燃烧;
⑵在通电条件下只有两种气体生成的分解反应。
运用溶解度表与溶解度曲线回答下列问题:
⑴B是的溶解度曲线。
⑵60℃时,100g水中加入100g硝酸钾,所得溶液是(填“饱和”或“不饱和”)溶液,当60℃的该溶液降温到30℃时,析出晶体的质量为g。
用化学符号填空:1个硫原子; 2个氮分子,我发现若化学符号前面的化学计量数大于1,则该符号只能表示(填“宏观”或“微观”)含义。
2009年12月7日在丹麦哥本哈根召开联合国气候会议,本次会议大力倡导"低碳经济。"低碳经济"是指在可持续发展理念指导下,尽可能地减少温室气体排放,达到经济社会发展与生态环境保护双赢的一种经济发展形态。
(1)
是常见的物质,某化学兴趣小组设计如图所示的各物质之间的转化关系图(部分反应的条件和产物略去),其中E是化学实验室中常用的燃料--酒精。请回答下列问颢:
①
的名称:。
②酒精燃烧产生
,但同学们认为用上图思路开发酒精燃料也符合"低碳经济"的要求,同学们的理由是。
(2)目前我国正大力研发电动汽车,制约电动汽车发展瓶颈的是电池的性能。科技人员已研制出一种新型电池一一锂空气电池,它能提供相当于普通锂电池10倍的能量。该电池在放电时锂(
)与水和空气中氧气反应生成氢氧化锂(
),该反应的化学方程式是:。
(3)作为一名中学生,我们也可以从身边的事情做起.响应"低碳生活"。请列举一个你可以做到的事情:。