在下列的电子结构中,第一电离能最小的原子可能是( )
| A.ns2np3 | B.ns2np5 | C.ns2np4 | D.ns2np6 |
利用右图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。下列说法正确的是
| A.a为直流电源的负极 |
B.阴极的电极反应式为:2HSO +2H++e-===S2O +2H++e-===S2O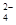 +2H2O +2H2O |
C.阳极的电极反应式为:SO2+2H2O-2e-===SO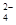 +4H+ +4H+ |
| D.电解时,H+由阴极室通过阳离子交换膜到阳极室 |
现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如下: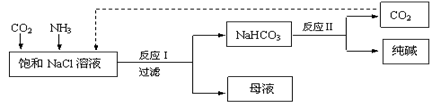
有关说法错误的是()
| A.反应Ⅰ原理为CO2 + NH3 + NaCl + H2O ="=" NaHCO3↓ + NH4Cl |
| B.向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3 |
| C.反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱 |
| D.往母液中通入氨气,加入细小的食盐颗粒并降温,可使氯化铵析出 |
海洋中有丰富的食品、矿产,能源、药物和水产资源等(如下图所示),
下列有关说法正确的是()
| A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为: Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.第②步中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2 |
| C.在第③④⑤步中溴元素均被氧化 |
| D.从第③步到第⑤步的目的是为了浓缩 |
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是()
| 选项 |
a中物质 |
b中物质 |
c中收集气体 |
d中物质 |
| A |
浓氨水 |
CaO |
NH3 |
H2O |
| B |
浓硫酸 |
浓盐酸 |
HCl |
NaOH溶液 |
| C |
稀硝酸 |
Cu |
NO2 |
H2O |
| D |
浓盐酸 |
MnO2 |
Cl2 |
NaOH溶液 |
X、Y、Z、W四种短周期元素在周期表中的相对位置如右图所示,其中X与W的质子数之和为21,由此可知()
| X |
Y |
||
| Z |
W |
A.X位于元素周期表中第2周期、第VA族
B.Y的氢化物(H2Y)不稳定,100℃以上即可分解
C.Z的最高价氧化物的水化物是一种强碱
D.W的非金属性比Y的非金属性弱