为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是( )
| |
被提纯的物质 |
除杂试剂 |
分离方法 |
| A |
乙醇(水) |
新制生石灰 |
蒸馏 |
| B |
苯(苯酚) |
浓溴水 |
过滤 |
| C |
二氧化碳(SO2) |
氢氧化钠溶液 |
洗气 |
| D |
溴苯(溴) |
氢氧化钠溶液 |
分液 |
“三酸二碱”在化工生产中有着重要的应用。下列说法正确的是
| A.在沸腾炉和接触室中,均使用过量的高压空气,以提高硫铁矿的燃烧利用率和二氧化硫的催化氧化转化率 |
| B.上图是工业制盐酸的设备及其简易图 |
| C.氯碱工业是中国现代化工之母,其主要反应是电解海水,得到烧碱和氯气,因此称为氯碱工业 |
| D.合成氨工业是工业制硝酸和工业制纯碱的前提和保证,前者可为后两者共提供了不止一种原料 |
室温下,在0.2 mol/LAl2(SO4)3溶液中,逐滴加入1.0 mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列说法正确的是
| A.a点,离子方程式为:Al3+ +3OH—→Al(OH)3↓ |
| B.a~b段,溶液pH增大,促进了氢氧化铝的碱式电离 |
| C.b~c段,加入的OH—主要用于生成Al(OH)3沉淀 |
| D.d点时,Al(OH)3沉淀开始溶解 |
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是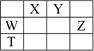
| A.X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B.由X、Y和氢三种元素形成的化合物中只有共价键 |
| C.原子得电子能力强弱:W<X<Y<Z |
| D.T元素的单质可能具有半导体的特性,T与Z元素可形成化合物TZ4 |
下列有关Fe2(SO4)3溶液的叙述正确的是
| A.该溶液中,K+、Fe2+、I—、Br—可以大量共存 |
| B.用该溶液中溶解一定量铜粉,向所得溶液中再加入铁粉,若溶液中有Cu2+,则一定没有固体析出 |
| C.将该溶液蒸干,得到的固体中混有氢氧化铁 |
| D.100mL 0.1 mol/L该溶液和足量的Zn充分反应,生成1.12 gFe |
Na2O2、Cl2和SO2均能使品红溶液褪色(NA为阿伏加德罗常数的值)。下列说法正确的是
| A.Na2O2、Cl2、SO2使品红溶液褪色的原理相同 |
| B.标准状况下,1 mol Na2O2和22.4LCO2反应,转移电子数目为NA |
| C.等物质的量的Cl2和SO2同时通入品红溶液中,品红褪色更快 |
| D.在Na2O2中阴阳离子所含的电子数目相等 |