(15分)某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
| 阳离子 |
K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 |
Cl- CO32- NO3- SO42- SiO32- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是 (写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的的离子方程式是_________________________。
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为
_______________________________________________________________
(4)甲同学最终确定原溶液中所含阳离子是 ,阴离子是 。(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为 g。
(6)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是
| 选项 |
污染物 |
处理措施 |
方法类别 |
| A |
废酸 |
加生石灰中和 |
物理法 |
| B |
Cu2+等重金属离子 |
加硫酸盐沉降 |
化学法 |
| C |
含复杂有机物的废水 |
通过微生物代谢 |
物理法 |
| D |
碱性的废水 |
用CO2来中和 |
化学法 |
(6分)有一固体混合物,可能由Na2CO3、K2SO4、CuSO4、Ca(NO3)2、KCl、AgNO3等混合而成,为检验它们,做了如下实验:①将固体混合物溶于水,搅拌后得无色透明溶液;②往此溶液中滴加BaCl2溶液,有白色沉淀生成;③过滤,将沉淀物置于足量稀硝酸中,发现沉淀全部溶解。试判断:
(1)固体混合物中肯定有,肯定没有,可能;(用化学式填写)
(2)写出实验③中发生的反应的离子方程式:。
a到g元素的原子最外层都是M层,最外层电子数如下:
| 元素 |
a |
b |
c |
d |
e |
f |
g |
| 最外层电子数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
用化学符号完成下列问题:
(1)元素b与元素g形成的稳定化合物,其电子式:
(2)在d、e、f、g所形成的气态氢化物中稳定性最差的是:
(3)工业制备单质d的化学反应方程式:
(4)元素c的最高价氧化物对应的水化物分别与元素a、f的最高价氧化物对应的水化物反应的离子方程式:①
②
(8分)如何用所提供的试剂和方法除去混合物中的杂质(括号内为杂质)。将所选答案的编号填入表内相应的空格中(不需要外加试剂的,此格可标“——”,可重复选择)
I.可供选择的试剂:
| A.盐酸 | B.NaOH溶液 | C.CuO | D.饱和的NaHSO3溶液 |
II.可供选用的操作:①洗气②加热③过滤④分液
| 混合物 |
所用试剂 |
主要操作 |
|
| (1) |
BaSO4(I2) |
||
| (2) |
CaCO3(SiO2) |
||
| (3) |
SO2(HCl) |
||
| (4) |
CO2(CO) |
根据图示填空
(1)化合物A含 有的官能团是、、。
有的官能团是、、。
(2)1mol A与2mol H2反应生成1molE,其反应方程式是
。
(3)与A具有相同官能团的A的同分异构体的结构简式是。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是。
(5)F的结构简式是。由E生成F的反应类型是。
下表是A、B、C、D、E五种有机物的有关信息: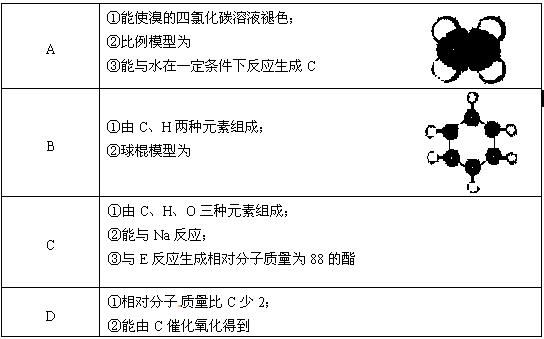
回答下列问题:
(1)A~E中,属于烃的是 (填字母)。
(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为
。
(3)C催化氧化生成D的化学方程式为
。
(4)有机物B具有的性质是(填序号)。
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计
一个实验来比较E与碳酸酸性的强弱,则该实验的原理是(用化学方程式说明)
。