a到g元素的原子最外层都是M层,最外层电子数如下:
| 元素 |
a |
b |
c |
d |
e |
f |
g |
| 最外层电子数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
用化学符号完成下列问题:
(1)元素b与元素g形成的稳定化合物,其电子式:
(2)在d、e、f、g所形成的气态氢化物中稳定性最差的是:
(3)工业制备单质d的化学反应方程式:
(4)元素c的最高价氧化物对应的水化物分别与元素a、f的最高价氧化物对应的水化物反应的离子方程式:①
②
某温度时,在2L密闭容器中某一反应中A、B物质的量随时间变化的曲线如图所示:
由图中数据分析并填写空格:
(1)该反应的化学方程式为______________________________。
(2)在0~4min时间内,A的平均反应速率为__________________________。
(3)4 min时,正、逆反应速率的大小关系为: (正)_____________
(正)_____________ (逆)(填“>”、“<”或“=”,下同)8 min时
(逆)(填“>”、“<”或“=”,下同)8 min时 (正)_____________
(正)_____________ (逆)
(逆)
把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:
3X(气) + Y(气) = nZ(气) + 2W(气) 5min末已生成0.2molW,若测知以Z浓度变化来表示的反应平均速率为0.01mol/(L·min)求:
(1)反应中Z气体的计量数n:
(2)反应在5分钟末时,Y的转化率:
(3)以X浓度变化来表示的反应平均速率为
已知A、B、C、D、E是短周期元素,它们的原子序数逐渐增大。A元素原子形成的离子没有电子;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)A的离子符号是________;
(2)C、D的最高价氧化物的水化物相互反应的离子方程式是________;
(3)A、B、C三种元素形成的化合物所含的化学键类型是________;
(4)B、C、D三种元素的离子半径由大到小的顺序是________。
已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液: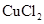 溶液、
溶液、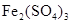 溶液、盐酸。按要求回答下列问题:
溶液、盐酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池
,若能,请写出电极反应式,负极,正极。(若不能,后两空不填)
(3)设计一种以铁和硫酸反应为原理的原电池,要求画出装置图:(需标明电极材料及电池的正负极)
按要求填空:
(1)写出下列反应的化学方程式:
①镁和水反应 ___________________________________________
②氧化铝和氢氧化钠溶液反应_______________________________________
③硅酸钠溶液露置在空气中变质 __________________________________________
(2)写出表示含有8个质子,10个中子的原子的化学符号:;
在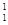 H、
H、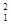 H、
H、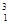 H中共有种原子,它们能形成种氢气分子。
H中共有种原子,它们能形成种氢气分子。
(3)某简单微粒的结构示意图为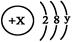 且X、Y 均为不大于20的正整数,据此回答下列问题:
且X、Y 均为不大于20的正整数,据此回答下列问题:
①若呈电中性时该微粒不易与其它物质发生反应,这种微粒的符号是;
②若该微粒为负一价阴离子,则x=,该元素的最高价氧化物的化学式为。
⑷某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧质量分数为60%。则该元素的气态氢化物化学式为。