某共价化合物含 C 、 H 、 N三元素 , 分子内有 4 个 N 原子 , 且 4 个 N 原子排列成内空的四面体 ( 如白磷分子结构 ), 每两个 N 原子间都有一个 C 原子 , 分子内无C-C单键和C=C双键。
(1) 试确定该化合物的分子式_____________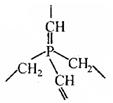
(2) 假若某大分子 , 分子内只含 C 、 H 、 P 二种元素 , 其最小的重复的结构单元如上图当该化合物分子中含n个磷原子时,则该化合物的组成可表示为____________________。
在一个1 L的密闭容器中,加入2 mol A和1 mol B,发生下列反应:2A(g)+B(g) 3C(g) + D(s), 达到平衡时,C的浓度为1.2 mol·L-1。
3C(g) + D(s), 达到平衡时,C的浓度为1.2 mol·L-1。
(1)维持容器的温度不变,若缩小容器的体积,则平衡__________移动(填“向正反应方向”“向逆反应方向”或“不”)。
(2)维持容器的体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍是1.2 mol·L-1的是__________________。
A.4 mol A+2 mol B
B.3 mol C+1 mol D
C.2 mol A+1 mol B+1 mol D
(3)若维持容器的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2 mol·L-1,则C的起始物质的量应满足的条件是_________________。
向一容积为5 L的密闭容器中充入NH3和O2,它们的物质的量之比为1∶2,发生如下反应:4NH3+5O2 4NO+6H2O(g)。
4NO+6H2O(g)。
(1)上述反应在一定条件下进行,2 min后该反应的ΔH-TΔS=0,此时该反应达到__________________状态,NH3为2 mol,NH3的转化率为20%。以NO的浓度变化表示该反应的平均反应速率为________________, O2的平衡浓度为_________________。
(2)在达到平衡后,充入相当于原组成气体1倍的惰性气体。如果容器的体积不变,平衡______________移动。
已知化学反应N2+3H2====2NH3的能量变化如图所示。
(1)1 mol N 和3 mol H 生成1 mol NH3(g)是_________________能量的过程(填“吸收”或“释放”)。
(2)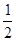 N2(g)+
N2(g)+ H2(g)====NH3(g) ΔH=_________________。
H2(g)====NH3(g) ΔH=_________________。
(3)N2(g)和H2(g)生成NH3(l)的热化学方程式____________________。
由化学能产生的能量是目前人类使用的主要能源。请回答下列问题:
(1)N2和O2在一定条件下反应生成NO2的热化学方程式为: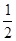 N2(g)+O2(g)====NO2(g) ΔH=+34 kJ·mol-1。该反应为_____________(“放热”“吸热”)反应。
N2(g)+O2(g)====NO2(g) ΔH=+34 kJ·mol-1。该反应为_____________(“放热”“吸热”)反应。
(2)化学反应中的能量变化源自于化学反应中化学键变化时产生的能量变化。下表为一些化学键的键能:
| 化学键 |
键能( kJ·mol-1) |
化学键 |
键能( kJ·mol-1) |
| N≡N |
942 |
H—O |
460 |
| N—H |
391 |
O==O |
499 |
| H—H |
437 |
①写出N2和H2反应合成氨的热化学方程式_________________________。
②已知:1 mol H2O(g)转化为1 mol H2O(l)时放出44.0 kJ的热量。计算1 g H2完全燃烧时放出的热量___________________。H2O(g)的稳定性___________(“大于”“小于”)H2O(l)。
(3)写出NH3(g)在O2(g)中完全燃烧生成NO2(g)和H2O(g)的热化学方程式_________________________________________________________________________。
在某一容积为5 L的密闭容器内,加入0.2 mol CO和0.2 mol H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图所示:
CO2(g)+H2(g) ΔH>0,反应中CO2的浓度随时间变化情况如图所示:
(1)根据图中数据,反应开始至达到平衡时,CO的化学反应速率为__________,反应达平衡时,c(H2)=__________。
(2)判断该反应达平衡的依据是__________(填序号)。
①CO减少的速率和CO2减少的速率相等
②CO、H2O、CO2、H2的浓度都相等
③CO、H2O、CO2、H2的浓度都不再发生变化
④该条件下正、逆反应速率都为零
(3)如果一开始加入0.1 mol的CO、0.1 mol的H2O、0.1 mol的CO2和0.1 mol的H2,在相同条件下,反应达平衡时,c(H2O)=__________。