常温下,ZnS的溶度积常数Ksp=1.20×10-23 ,H2S的电离常数K1=1.32×10-7 K2=7.10×10-15 回答下列问题:
(1)K1>>K2的原因是
(2)0.1 mol/L H2S溶液中氢离子的物质的量浓度是 (填字母)
| A.等于0.1mol/L | B.等于0.2mol/L |
| C.小于0.1mol/L | D.在0.1~0.2mol/L之间 |
(3)0.1mol/LNa2S 溶液能使pH试纸变蓝,表明该现象的离子方程式是
(4)已知0.1mol/LNaHS溶液的pH约为9,则0.1mol/LNaHS溶液中各离子浓度由大到小的顺序是 。该溶液中的质子守恒关系式为
。
(5)向0.01mol/L的ZnCl2溶液中通入H2S(g)至饱和(c(H2S)按0.1mol/L计),为保证不产生ZnS沉淀,应控制c(H+)不低于 mol/L(已知7.811/2 =2.8)
(1)向盛有25 mL 0.2 mol /L的Na2CO3溶液的试管中缓缓滴入0.1 mol /L盐酸75 mL,且边加边振荡,则在标况下产生CO2气体的体积为mL
(2)FeCl3溶液中混有FeCl2,写出除杂试剂的化学式为;反应的离子方程式为
(3)FeCl2溶液中混有FeCl3,写出能检验杂质离子的离子方程式
(4)2.1克平均式量为7.2的CO和H2组成的混和气体在足量的氧气中充分燃烧后,立即通入足量的Na2O2粉未中,待反应完全后,粉末质量可增加g
(5)1mol Na2O2与足量的CO2完全反应,转移电子的物质的量为
(6)Fe(OH)2转化为Fe(OH)3的现象为化学方程式为
晶体是质点(分子、离子、或原子)在空间有规则地排列的,具有整齐外形,以多面体出现的固体物质。在空间里无限地周期性的重复能成为晶体的具有代表性的最小单元,称为晶胞。一种Al-Fe合金的立体晶胞如图所示。
⑴确定该合金的化学式____________。
⑵若晶胞的边长为a nm,阿伏加德罗常数为NA,则此合金的密度为_____________g/cm3。(化为最简)
⑶取一定质量的该合金粉末溶于足量的稀NaOH溶液中,待反应完全停止后得到气体6.72 L。过滤,将残渣用蒸馏水洗净后,取其质量的十分之一,投入100mL一定浓度的稀硝酸中,恰好完全反应,共收集到气体0.672L。(气体体积均在标准状况下测定)
①计算硝酸的物质的量浓度。
②最终所得溶液中Fe3+的物质的量浓度(假设溶液体积仍为100mL)。
(1)确定该合金的化学式____________
(2)__________________g/cm3(化为最简)
(3)__________________________________________
①
____________________________
②
___________________________。
磷单质及其化合物有广泛应用。
(1)三聚磷酸可视为三个磷酸分子(磷酸结构式见右图)之间脱去两个分子产物,
其结构式为___________。三聚磷酸钠(俗称“五钠”)是常用的水处理剂,
其化学式为____________。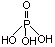
(2)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为______________。
②化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)____ Ni2++____ H2PO2-+____→____ Ni+____ H2PO3-+____
(b)6H2PO2-+2H+=2P+4H2PO3+3H2
请在答题卡上写出并配平反应式。
③利用②中反应可在塑料镀件表面沉积镍-磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。
方法上的不同点____________________,原理上的共同点____________________,
化学镀的优点______________________。
(1)下列数据是对应物质的熔点(℃)
| NaCl |
Na2O |
AlF3 |
AlCl3 |
BCl3 |
Al2O3 |
CO2 |
SiO2 |
| 801 |
920 |
1291 |
190 |
-109 |
2073 |
-57 |
1723 |
据此作出的下列判断中,错误的是
A、铝的化合物晶体 中有离子晶体
中有离子晶体
B、表中只有BCl3、干冰是分子晶体
C、同族元素的氧化物可形成不同类型的晶体
D、不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图所示。SiO2晶体中Si和Si-O键的比例为_____________。
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。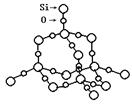
| 化学键 |
Si-O |
Si-Si |
O=O |
| 键能/ KJ·mol-1 |
460 |
176 |
498 |
Si(s)+O2(g) SiO2(s),该反应的反应热△H =" ___________"
SiO2(s),该反应的反应热△H =" ___________"
(1)下列物质在固态时,属于分子晶体的有,属于原子晶体的,属于离子晶体的有。①金刚石②氩③水 晶④水银⑤氧化铝⑥P4⑦苯
晶④水银⑤氧化铝⑥P4⑦苯
(2)比较下列物质的有关性质(用“>、<、=或≈”号连接)
沸点:16O218O2熔点:NaK稳定性:H2OD2O
(3)某常见固体能导电,质软,它可能属于__________
| A.分子晶体 | B.原子晶体 | C.离子晶体 | D.金属晶体E.混合晶体 |
(4)在氯化铯晶体(见图1)中,若以某一铯离子为球心,与之等距离的若干离子构成
一个球面。与某铯离子距离最近的离子构成的球面(最内层的球面或第一层球面)
上有个离子(填写离子符号,下同),第二层球面上有个
离子。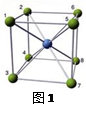
(5)在氯化钠晶体(见图2)中,每个钠离子与个最近且等距离的氯离
子以键相结合,与每个氯离子最近的且等距离的氯离子有个。
由于晶体中离子按一定的规律排列,必然造就了一颗完美晶体特定的几何外形,
其中,氯化钠单晶的 宏观外形为。
宏观外形为。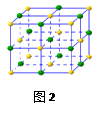
元素代 号 号 |
I1 |
I2 |
I3 |
I4 |
| Q |
2080 |
4000 |
6100 |
9400 |
| R |
500 |
4600 |
6900 |
9500 |
| S |
740 |
1500 |
7700 |
10500 |
| T |
580 |
1800 |
2700 |
11600 |
| U |
420 |
3100 |
4400 |
5900 |