1mol/L H2SO4的含义是
| A.1L水中溶解1mol H2SO4 |
| B.1L溶液中含有1molH+ |
| C.将98g H2SO4溶于1L水中配成溶液 |
| D.1L H2SO4溶液中含有98gH2SO4 |
常温下,把pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系正确的是()
| A.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | B.c(Na+)+c(H+)>c(CH3COO-)+c(OH-) |
C.c(CH3COO-)>c (Na+)>c(H+)=c(OH-) (Na+)>c(H+)=c(OH-) |
D.c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
若溶液中由水电离产生的c(OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是()
A Al3+Na+NO-3 Cl- B K+ Na +Cl- NO3-
+Cl- NO3-
C K+ Na+ Cl-AlO2- D K+ NH+4 SO42-NO3-
下列对熵的理解不正确的是( )
| A.同种物质气态时熵值最大,固态时熵值最小 |
| B.体系越有序,熵值越小;越混乱,熵值越大 |
| C.与外界隔离的体系,自发过程将导致体系的熵减小 |
| D.25 ℃、1.01×105 Pa时,2N2O5(g) =4NO2(g)+O2(g)是熵增的反应 |
下列离子方程式书写正确的是()
| A.Na2HPO4溶于水:Na2HPO4=2Na++H++PO43- |
| B.NaHCO3溶液的水解离子方程式:HCO3- + H2O = H3O+ + CO32- |
C.HF溶 于少量水中: 2HF=H++HF2一 于少量水中: 2HF=H++HF2一 |
| D.(NH4)2 SO4溶于水:(NH4)2 SO4=2 NH4++SO42一 |
在密闭容器中,反应X2(g) +Y2(g)
+Y2(g) 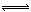 2XY(g);ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是()
2XY(g);ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是()
A.图Ⅰ是加入适当催化剂的变化情况   |
B.图Ⅱ是扩大容器体积的变化情况 |
| C.图Ⅲ是增大压强的变化情况 | D.图Ⅲ是升高温度的变化情况 |