某化学研究小组在使用FeSO4 溶液与NaOH溶液制备Fe(OH)2沉淀过程中观察到生成的白色沉淀迅速转变为灰绿色,最后变为红褐色。该小组针对绿色物质展开研究。
[查阅文献]
| 文献名称 |
有关Fe(OH)2的描述 |
| 《大学普通化学(下册)》 |
白色沉淀,易被氧化成微绿色Fe3(OH)8 |
| 《化学教育》 |
其水合物Fe(OH)2·nH2O呈绿色,热溶液中不易形成水合物 |
写出Fe(OH)2 在空气中被氧化为Fe3(OH)8 的化学方程式 。
[提出假设]假设一:绿色物质是Fe(OH)2·nH2O;
假设二:_______________________。
……
[实验探究]针对上述假设一与假设二,展开实验研究:
| 实验序号 |
实验步骤 |
实验现象 |
| 一 |
①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ②保持较高温度,使用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液 |
出现白色絮状沉淀,并能保持一段时间 |
| 二 |
①在试管中加入20mL蒸馏水 ②加入一滴饱和FeSO4 溶液、一滴NaOH溶液 |
出现白色沉淀,迅速转变为灰绿色,最后变为红褐色 |
| 三 |
①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ②恢复室温后,使用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液 |
出现白色沉淀,迅速转变为绿色沉淀 |
(1)实验室保存FeSO4溶液常需加入 、 。
(2)由实验一与实验 (填实验序号)的现象可推断假设 可能成立。
(3)为了进一步探究假设二是否成立,小组成员进行如下实验,请完成下表:
试剂:蒸馏水、NaOH溶液、苯、FeSO4溶液、氧气
| 实验步骤 |
实验现象与结论 |
| ①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ②迅速 得到白色沉淀Fe(OH)2 ③ 。 |
若沉淀中出现绿色的迹象,则假设二成立; 若沉淀中没有出现任何绿色的迹象,则假设二不成立。 |
实验题:某学生为了验证氢气还原氧化铜的产物,设计了下图所示的实验装置。
⑴ 写出编号仪器的名称: ①______________
⑵ 写出A中反应的离子方程式_____________________________
⑶ 浓H2SO4的作用是_____________________
⑷ 本实验需要加热的装置为____________(填字母编号)。
⑸ 写出装置C、D中可观察到的现象:C______ ___,D_________
⑹ D中反应每生成1mol水分子,转移的电子数为____________个。
(9分)某非金属单质A经如下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题: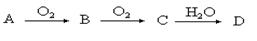
(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体。
①A、D的化学式分别为:AD
②工业生产中大量排放的B气体被雨水吸收后形成而污染环境。
③写出B→C反应的化学方程式:
(2)若A在常温下为气体,C是红棕色气体。
①A的电子式为,C的化学式为
②写出C→D反应的化学方程式:
在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在
铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花。给试管加热,观察现象。反应一段时间后,停止加热。回答下列问题: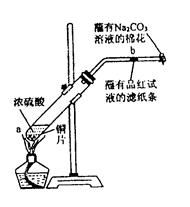
(1)写出a处反应的化学方程式。
(2)试管中的液体反应一段时间后,b处滤纸条的变化为。待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为。
(3)待试管中的液体冷却后,将试管上层液体倒去,再将剩余物质慢慢加入水中,可观
察溶液呈色。
(4)玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花所起的作用是,反应
的化学方程式为。
(5)若用浓度为18 mol/L的浓硫酸100 mL与过量的铜片,加热使之反应,则被还原的硫酸(选填“大于”、“等于”或“小于”)0.9 mol 。
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
(1)甲同学研究的实验报告如下表:
| 实验步骤 |
现象 |
结论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 |
反应快慢: Mg>Fe>Cu |
反应物的性质越活泼,反应速率越快。 |
该同学的实验目的是研究____________对反应速率的影响;根据控制变量法,要得出正确的实验结论,还需控制的实验条件是保持______________条件相同。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品是_____________;应该测定的实验数据是________________________。
实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是______________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是______。
A、硫酸钾 B、硫酸锰 C、水 D、氯化锰
某研究性学习小组用FeCl3溶液做“腐蚀液”,制作印刷电路板,其反应原理是:2FeCl3+Cu=2FeCl2+CuCl2。
【实验探究】
(1)通过《化学1》的学习,知道了有离子参加的化学反应为离子反应。离子反应可用离子方程式表示。请写出2FeCl3+Cu=2FeCl2+CuCl2反应的离子方程式为:。
(2)若要溶解电路板上3.2g的铜,则至少需要FeCl3物质的量为mol。
(3)使用后失效的“腐蚀液”为废液,验证废液中是否存在Fe3+的试剂是,加入该试剂后,若出现现象,说明废液中还存在Fe3+。
(4)废液中的CuCl2可通过加入足量的,反应后转化成铜且能使所得溶液中含有单一溶质。
(5)回收Cu后的废液,通入足量的Cl2,可以重新获得FeCl3溶液,其反应的化学方程式为。
【实验结论】
利用FeCl3溶液做印刷电路板的“腐蚀液”,不仅废液中的铜可以得到回收,经过处理后的废液还可以重新使用。
【知识拓展】
(6)铁元素是维持生命活动不可缺少的微量元素,虽然人体中通常只含有3~5g铁元素,但铁元素在人体中却发挥着重要作用,人体缺铁会引起疾病。