在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
| 温度/℃ |
25 |
80 |
230 |
| 平衡常数 |
5×104 |
2 |
1.9×10-5 |
下列说法不正确的是
A.上述生成Ni(CO)4(g)的反应为吸热反应
B.25°C时反应Ni(CO)4(g) Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
C.80°C达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L
D.80°C时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)
双酚A作为食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。下列有关双酚A的叙述不正确的是
| A.双酚A的分子式是C15H16O2 |
| B.反应①的反应类型是加成反应 |
| C.反应②的产物能与Na发生置换反应 |
| D.双酚A中所有原子不可能共面 |
将一定质量的铜粉加入到100mL某浓度的稀硝酸中,充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体448mL(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器剩有铜粉m2g,则(m1-m2)为
| A.5.76 | B.2.88 | C.1.92 | D.0 |
下列叙述正确的是:①用氨水清洗做过银镜反应的试管;②用分液漏斗分离硝基苯和水的混合物;③用pH试纸测定新制氯水的pH;④用碱式滴定管量取20.00mL 0.1
mol/LKMnO4溶液;⑤不慎将苯酚溶液沾到皮肤上,立即用NaOH稀溶液清洗;⑥含有离子键的化合物一定为离子化合物;⑦用托盘天平准确称取29.25gNaCl配制500mL 0.1mol/L的NaCl溶液;⑧Na2CO3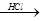 CO2
CO2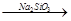 白色沉淀,说明元素的非金属性:Cl>C>Si;⑨从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶;⑩胶体和溶液的本质区别是分散剂微粒直径的不同。
白色沉淀,说明元素的非金属性:Cl>C>Si;⑨从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶;⑩胶体和溶液的本质区别是分散剂微粒直径的不同。
| A.②⑥⑩ | B.①③④⑤⑧ | C.②⑥ | D.③④⑤⑥⑦⑨ |
中学化学教材中有大量数据,下列是某同学对数据的利用情况,其中正确的是
| A.利用焓变的数据或熵变的数据一定都能单独判断反应是否能自发进行 |
| B.利用反应热数据的大小判断不同反应的反应速率的大小 |
| C.利用沸点数据推测将一些液体混合物分离开来的可能性 |
| D.利用溶液的pH与7的大小关系,来判断任何温度下溶液的酸碱性 |
已知阿伏加德罗常数的值为NA,下列说法正确的是
A.1mol (甲基碳正离子)含有的电子数目为9NA (甲基碳正离子)含有的电子数目为9NA |
| B.标准状况下,2.24L甲苯含有的碳原子数目为0.7NA |
| C.6.2g氧化钠和7.8g过氧化钠的混合物中含有的离子总数为0.6NA |
| D.1molHCl气体中的粒子数与0.5mol·L-1盐酸中溶质粒子数相等 |