某同学测得物质的量浓度均为0.01mol/LCH3COOH和CH3COONa混合溶液呈酸性后,得出了关系式,你认为其中不正确的是
| A.c(CH3COO—)>c(CH3COOH) |
| B.c(CH3CO0—)>c(Na+)>c(H+)>c(OH—) |
| C.c(Na+)=c(CH3COO—)=0.01mol/L |
| D.c(CH3COOH)+c(CH3COO—)=0.02mol/L |
下列各组离子中,能在溶液中大量共存的是
| A.OH-Na+HCO3- Cl- | B.Ba2+ Na+Cl- SO42- |
| C.K+ Al3+ SO42-OH- | D.Ag+ Al3+ NO3-H+ |
从氧化还原角度分析,下列反应中水的作用相同的是
① 铁和水蒸气反应 ② 过氧化钠和水反应
③氯气和水反应 ④ 二氧化氮和水反应3NO2+H2O=2HNO3+NO
| A.①②③ | B.①②④ | C.②③④ | D.①③④ |
一些装有化学物质的容器上常贴有危险化学品的标志。下列化学药品名称与警示标志对应正确的是
A.酒精  |
B.浓硫酸 |
C.过氧化钠 |
D.四氯化碳 |
下列装置或操作能达到实验目的的是

| A.取4 g NaOH加入96 mL水中 | B.配制150mL0.10mol/L盐酸 配制4 % NaOH溶液  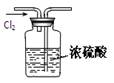 |
| C.读取液体体积 | D.干燥Cl2 |
当光束通过下列分散系时,能观察到丁达尔效应的是
| A.蔗糖溶液 | B.盐酸 | C.氯化钠溶液 | D.氢氧化铁胶体 |