在一密闭容器中,反应aA(g)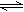 bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来平衡时的60%,则下列说法不正确的是( )
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来平衡时的60%,则下列说法不正确的是( )
| A.平衡向正反应方向移动了 | B.物质A的转化率增大了 |
| C.物质B的质量分数增加了 | D.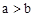 |
下列表格中的对应关系正确的是
有机物甲的分子式为C7H12O2,是一种六元环状酯,且甲的分子中含有2 个甲基,则甲的可能结构有
| A.6 种 | B.8 种 | C.10 种 | D.14 种 |
下列有关化学用语的表示正确的是
A.钠原子的结构示意图为 |
B.过氧化氢的电子式为 |
C.聚乙烯的结构简式为 |
| D.淀粉和纤维素的实验式都为CH2O |
氯化钠是海水的主要成分,也是人类生活中不能缺少的一种物质。下列关于氯化钠的说法正确的是
| A.氯化钠溶液能导电,所以氯化钠溶液是电解质 |
| B.氯化钠溶液可杀菌,说明氯化钠溶液具有强氧化性 |
| C.电解熔融氯化钠和电解氯化钠溶液的产物相同 |
| D.加碘食盐是指添加了碘的化合物的氯化钠 |
食品干燥剂应无毒、无味、无腐蚀性及环境友好。下列说法错误的是
| A.硅胶可用作食品干燥剂 |
| B.P2O5不可用作食品干燥剂 |
| C.六水氯化钙可用作食品干燥剂 |
| D.加工后具有吸水性的植物纤维可用作食品干燥剂 |