中科院大气研究所研究员张仁健课题组与同行合作,对北京地区PM2.5有6个重要来源,其中,汽车尾气和燃煤分别占4%、18%。用于净化汽车尾气的反应为2NO(g)+2CO(g) 2CO2(g)+N2(g),已知该反应在570K时平衡常数为1×1059,但反应很慢。下列说法正确的是( )

| A.装有尾气净化装置的汽车排出的气体中不再含有NO或CO |
| B.提高尾气净化效率的常用方法是升高温度 |
| C.增大压强,上述平衡右移,故实际操作中可通过增压的方式提高其净化效率 |
| D.提高尾气净化效率的最佳途径是使用高效催化剂 |
下列解释原理的表达式中,不正确的是()
A.镁的冶炼: 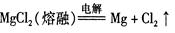 |
B.用热的纯碱溶液清洗油污: |
C.用Na2CO3溶液处理水垢中的CaSO4: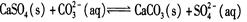 |
D.用氢氟酸刻蚀玻 璃:4HF+SiO2=SiF4↑+2H2O 璃:4HF+SiO2=SiF4↑+2H2O |
下列生产或实验中,所选用的酸合理的是()
| A.用浓盐酸和“84消毒液”制备氯气 |
| B.做焰色反应实验时,用稀硫酸洗涤镍铬丝 |
| C.在工业生产中用银和浓硝酸反应制取硝酸银 |
| D.在盐酸酸化的溶液中,PbO2将Mn2+氧化成MnO4- |
下列说法不正确的是()
| A.Al2O3用作耐火材料、Al(OH)3用作阻燃剂 |
| B.通过化学变化可以实现12C与14C间的转化 |
| C.碳素钢的主要成分是铁碳合金、司母戊鼎的主要成份是铜锡合金 |
| D.自然界中不存在游离态的硅,硅主要以二氧化硅和硅酸盐的形式存在 |
下列说法正确的是()
| A.SO2能使酸性KMnO4溶液迅速褪色 |
| B.可以用澄清石灰水鉴别SO2和CO2 |
| C.硫粉在过量的纯氧中燃烧可以生成SO3 |
| D.少量SO2通过浓的CaCl2溶液能生成白色沉淀 |
下列物质能通过化合反应直接制得的是()
①FeCl2 ②H2SO4③NH4NO3④HCl ⑤Fe(OH)3
| A.只有①②③ | B.只有②③ | C.只有①③④ | D.全部 |