在密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g) 2C(g);ΔH<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
2C(g);ΔH<0。达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是
| X |
Y |
|
| A |
再加入A |
B的转化率 |
| B |
再加入C |
A的体积分数 |
| C |
减小压强 |
A的转化率 |
| D |
升高温度 |
混合气体平均摩尔质量 |
可逆反应:3 A(g) 3 B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是
3 B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是
A.B和C可能都是固体B.B和C一定都是气体
C.若C为固体,则B一定是气体 D.B和C可能都是气体
用来表示可逆反应2A(g) + B(g) 2C(g) ;△H<0的正确图像为
2C(g) ;△H<0的正确图像为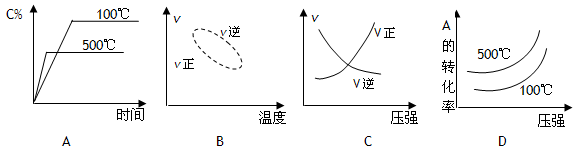
已知一定温度下合成氨反应:N2 +3 H2 2 NH3 (每生成2 mol NH3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol N2和3 mol H2,达平衡时放出热量为Q1,②通入2 mol N2和6 mol H2,达平衡时放出热量为Q2,则下列关系正确的是
2 NH3 (每生成2 mol NH3放出92.4 kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1 mol N2和3 mol H2,达平衡时放出热量为Q1,②通入2 mol N2和6 mol H2,达平衡时放出热量为Q2,则下列关系正确的是
| A.Q2 =" 2" Q1 | B.Q1 < 0.5 Q2 | C.Q1 < Q2 < 184.8 kJ | D.Q1 = Q2 < 92.4 kJ |
在一定温度下,把2. 0体积的N2和6. 0体积的H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:N2+3H2 2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是
2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是
| A.1.0体积的N2和3.0体积的H2 |
| B.2.0体积的N2、6.0体积的H2和4.0体积的NH3 |
| C.2.0体积的NH3 |
| D.4.0体积的NH3和1.0体积的H2 |