石灰石是一种重要的矿产,小江同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验。
| 实验步骤 |
①称取烧杯的质量 |
②将适量盐酸加入烧杯中并称重 |
③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 |
④待反应完全后,称重 |
| 实验图示 |
 |
|||
| 实验数据 |
烧杯的质量为50.0g |
烧杯和盐酸的质量为100.0g |
石灰石样品样品的质量为12.0g |
烧杯和其中混合物的质量为107.6g |
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是多少克?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与盐酸反应也不溶于水)
某硫酸钠样品中含有少量氯化钠。取15 g该样品于烧杯中,加入50 g水后完全溶解。向烧杯中滴加208.3 g氯化钡溶液,恰好完全反应,过滤、干燥,称得固体物质的质量为23.3 g。请计算
已知:BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl
(1)硫酸钠样品中氯化钠的质量
(2)若将滤液的溶质质量分数变为10%,需蒸发掉水的质量
)氢气是未来汽车的理想燃料。利用合适的催化剂和光能将水分解是制取氢气最理想的办法。若利用此方法分解36 Kg水,请计算理论上能产生氢气的质量。
请根据下图所示的实验过程和提供的数据,解答下列问题: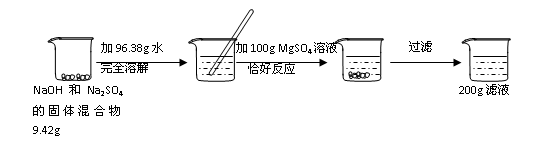
小提示:2NaOH+ MgSO4→ Na2SO4 + Mg(OH)2↓;
Na2SO4溶液不与MgSO4溶液发生反应。
(1)实验过程中,产生沉淀的质量为 g。
(2)最终所得溶液的溶质质量分数为多少?(写出计算过程)
(3)原固体混合物中钠元素的质量为g。
二氧化碳是一种宝贵的碳氧资源。它可以与氢气反应生成多种有机物,CO2转化为乙烯(C2H4)的化学方程式为:2CO2+6H2一定条件C2H4+ 4H2O。若用12t H2参与反应,则理论上能生成C2H4的质量为多少t ?
市场上某补钙制剂的说明书如图所示,
请计算:
(1)葡萄糖酸钙的相对分子质量为 。
(2)葡萄糖酸钙中碳、氢、氧、钙四种元素的质量比为。
(3)葡萄糖酸钙中钙元素的质量分数为(保留至0.1%)
(4)按照说明书的用量,每天可补充mg钙元素?(精确到0.1)