(本题共12分)
Ⅰ、氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)氮元素原子的L层电子数为 ;
(2) NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g) = N2O4(l) ΔH1=-19.5kJ∙mol-1
②N2H4(l) + O2 (g)=N2(g)+2H2O(g) ΔH2 ="-534.2" kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 。
Ⅱ、一定质量的液态化合物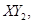 在标准状况下的一定质量的
在标准状况下的一定质量的 中恰好完全燃烧,反应方程式为:
中恰好完全燃烧,反应方程式为: ===
=== 冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56
冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56  则:
则:
(1)反应前 的体积是 。 (2)化合物
的体积是 。 (2)化合物 的摩尔质量是 。
的摩尔质量是 。
(3)若 分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为 和 (写元素符号)。
分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为 和 (写元素符号)。
(1)在标准状况下,4.8g甲烷(CH4)所占的体积为_________L,它与标准状况下________L硫化氢(H2S)含有相同数目的氢原子;
(2)等质量的甲烷与铵根所含的电子数之比______,质子数之比。
(2分)在KCl、ZnCl2、ZnSO4三种盐配成的混合溶液中,已知K+为0.1mol、Zn2+为0.25mol,Cl-为0.2mol,则SO42-为mol.
(8分)有以下几种物质①熔融氯化钠②液态氯化氢③Cu④蔗糖⑤KAl(SO4)2⑥NaHCO3溶液,填空回答:(填序号)
(1)以上物质中属于电解质的是; 属于非电解质的是;能导电的是。
(2)写出⑤的电离方程式:。
下图装置B中是浓度均为0.1mol/L的NaCl、CuSO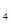 混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加____________g;此时,所有电极上总共收集到的气体的总体积为___________L(换算成标准状况下的体积)。
混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加____________g;此时,所有电极上总共收集到的气体的总体积为___________L(换算成标准状况下的体积)。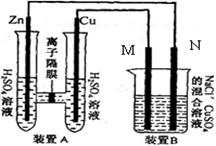
某学习小组用右图装置进行了有关电化学的实验。在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体,装置如图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅拌棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。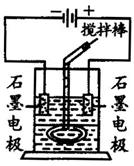
根据上述实验回答:
(1)阳极上的电极反应式为_______________________。
(2)环状玻璃搅拌棒的作用是______________________。
(3)原上层液体是___________。
(4)原下层液体是___________。
(5)搅拌后两层液体颜色发生变化的原因是:___________________________________________。
(6)要检验上层液体中含有的金属离子,其方法是__________,现象是___________________。