有一处于平衡状态的反应:X(s)+3Y(g) 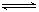 2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z(g) ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
| A.①③⑤ | B.②③⑤ | C.②③⑥ | D.②④⑥ |
下列物质无法从海水中获得的是
| A.硫酸 | B.氯化镁 | C.溴 | D.氢氧化钠 |
恒温条件下,往容积为2L的密闭容器内加入0.4 mol的N2和一定量的H2,在一定条件下发如下反应: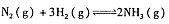 ,反应中NH3物质的量变化情况如下图:下列说法合理的是
,反应中NH3物质的量变化情况如下图:下列说法合理的是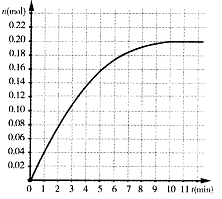
A.反应前l0min反应速率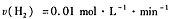 |
| B.N2平衡转化率为50% |
| C.若平衡时气体总压强为开始时的80%,则12min时氨气的体积分数为25% |
| D.其它条件不变,若改用5L容器达到平衡需 |
要的时间将小于l0min
某同学为研究电化学原理,使用KC1盐桥设计如图所示实验装置。下列分析不合理的是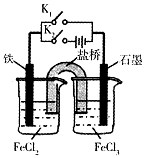
| A.闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动 |
B.无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是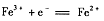 |
| C.闭合K,断开K2,电流从石墨电极经过K.流向铁电极 |
| D.闭合K,断开K2,左侧烧杯中的溶液pH将逐渐降低 |
常温下,0.1 mol·L-1CH3COONa溶液pH =a,则下列说法正确的是
| A.CH3COOH在常温下Ka数值约为l×101-2a |
| B.约有1.0×l0a-14 mol·L-1的水发生电离 |
| C.加热后溶液pH <a |
| D.加少量水后,溶液pH >a |
四种短周期元素在周期表中的相对位置如下图所示,其中Y为空气中含量最大的元素。下列叙述合理的是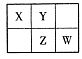
| A.元素W位于第三周期第ⅦA族 |
| B.Y、Z都是植物必需的元素 |
| C.原子半径:W>Z>Y>X |
| D.X氧化物的大量排放导致化学烟雾 |