[选做题]本题包括A、B两小题,分别对应于 “物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.铁是地壳中含量较丰富的元素,仅次于氧、硅、铝元素,其单质及合金是在生产生活中应用广泛的金属材料。化学上常用KSCN溶液等来检验溶液中是否存在Fe3+。
(1)Fe3+离子基态的电子排布式可表示为 。
(2)一种铁晶体的晶胞属于体心立方堆积,则该晶胞中所包括的铁原子的个数是 。
(3)C、N两种元素的简单气态氢化物的热稳定性由强到弱的顺序为 。
(填化学式)
(4)C、N、O三种元素的第一电离能由大到小的顺序为 。(填元素符号)
(5)离子化合物Fe2O3的熔点高于KC1的熔点的原因是 。
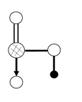
(6)据报道:由Q、X、Z三种元素形成的一种晶体具有超导性,其晶体结构如右图所示。晶体中距每个X原子周围距离最近的Q的原子的个数是 。
我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:
这种材料可采用如下图所示的合成路线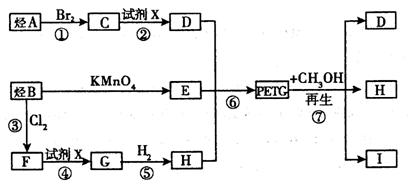
(1)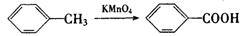
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1)⑦的反应类型是 。
(2)写出I的结构简式: 。
(3)合成时应控制的单体的物质的量:n(H):n(E):n (D)=(用m、n表示)。
(4)写出反应②的化学方程式:
(5)写出同时符合下列两项要求的E的所有同分异构体的结构简式。
①该同分异构体的苯环上相邻的三个碳原子上都连有取代基。
②该同分异构体在一定条件下能发生银镜反应和水解反应,遇到FeCl3溶液显紫色。
、 、 。
有机化学反应因反应条件不同,可生成不同的有机产品。例如: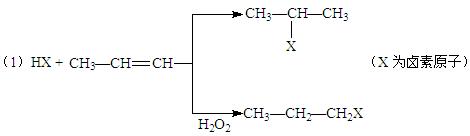
(2)苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
工业上利用上述信息,按下列路线合成结构简式为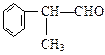 的物质,该物质是一种香料。
的物质,该物质是一种香料。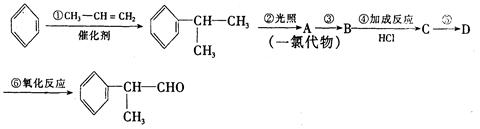
请根据上述路线,回答下列问题:
(1)A的结构简式可能为____________________________________。
(2)反应①、③、⑤的反应类型分别为________、________、_______。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):
_________________________________________________________。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,其原因是_____________________________________________。
(5)这种香料具有多种同分异构体,其中某些物质有下列特征: ①其水溶液遇FeCl3溶液呈紫色 ②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写两种):_________________________________________________。
①其水溶液遇FeCl3溶液呈紫色 ②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写两种):_________________________________________________。
某有机物X的蒸气完全燃烧时需要4.5倍于其体积的氧气,产生3倍于其体积的CO2和4倍于其体积的水蒸气。
(1)若该有机物的核磁共振谱有4个信号,则其结构简式为,其具有相同官能团的同分异构体的核磁共振谱有个信号。
(2)研究发现,当不对称烯烃与卤化氢发生加成反应时,通常“氢加到含氢多的不饱和碳原子一侧”。如:CH3CH=C(CH3)2 + HBr → CH3CH2CBr (CH3)2
若:①X的蒸气在Cu的催化下被氧气氧化成Y(Y分子属于酮类);②X能脱水生成烯烃Z,Z能和HCl反应主要生成有机物S;③S和NaOH水溶液共热,生成溶于水的有机物X。则:①写出X的名称;②用化学方程式表示①~③的转化过程。
①:
②:
③:
①化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号)。
①与金属钠反应 ②水解反应 ③加聚反应 ④与溴水反应 ⑤与碳酸钠反应
②已知,1,3—丁二烯的一类二烯烃能发生与具有双键的化合物进行1,4—加成反应生成环状化合物,这类反应称为双烯合成,例如: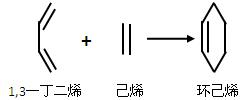
在下列横线上写出适当的反应物或生成物的键线式,完成下列反应: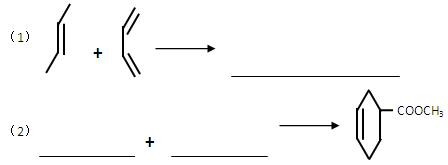
下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。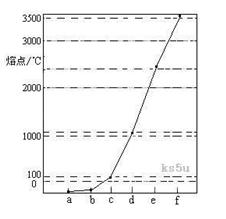
(1)请写出上图中d单质对应元素原子的电子排布式。
(2)单质a、f对应的元素以原子个数比1 :1形成的分子(相同条件下对H2的相对密度为13)中含个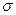 键和个
键和个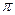 键。
键。 (3)a与b的元素形成的10电子中性分子X的空间构型为;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到络离子的化学式为,其中X与Ag+之间以键结合。
(3)a与b的元素形成的10电子中性分子X的空间构型为;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到络离子的化学式为,其中X与Ag+之间以键结合。
(4)下图是上述六种元素中的一种元素形成的含氧酸的结构:请简要说明该物质易溶于水的两个数原因。