自2010年8月7日,甘肃省舟曲县发生特大泥石流后,各地的救援物资远远不断运往灾区。下图为地方捐助的一种国家准字号补铁补血用药——复方硫酸亚铁叶酸片,其主要成分是绿矾——硫酸亚铁晶体(FeSO4·7H2O)
Ⅰ、某校课外活动小组为测定该补血剂中铁元素的含量特设计实验步骤如下: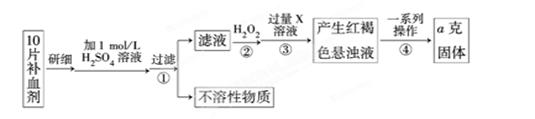
请回答下列问题:
(1)步骤②中加入过量H2O2的目的是 。
(2)步骤③中反应的离子方程式为 。
(3)步骤④中一系列处理的操作步骤是:过滤、 、灼烧、 、称量。
(4)若实验无损耗,则每片补血剂含铁元素的质量为 g(用含a的代数式表示)。
Ⅱ、灾难过后,灾区的饮用水变得非常的浑浊,不能饮用。因此对污染的饮用水的处理成了非常重要的事,其中处理的方法有很多:
(1)可以用适量绿矾和氯气一起作用于污染的自来水,而起到较好的净水效果;理由是(用离子方程式表示) 。
(2)在使用过程中发现绿矾和氯气的混合使用对酸性废水中的悬浮物处理效果较差,其原因是 。
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下: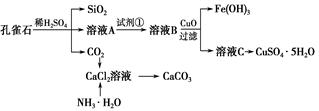
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为________(填代号),检验溶液A中Fe3+的最佳试剂为________(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、________、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是___________。
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。若实验过程中有氨气逸出,应选用下列________(填代号)装置回收。
(18分) “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
(1)乙醇、乙酸分子中的官能团分别是、
(2)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
(3)该反应属于哪类反应类型。
| A.加成反应 | B.取代反应 |
| C.水解反应 | D.酯化反应 |
E.可逆反应
(4)写出制取乙酸乙酯的化学反应方程式
。
(5)无水乙酸又称冰醋酸(熔点16.6℃)。在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸?
。
(6)乙醇在一定条件下还能发生脱水反应产生乙烯。乙烯通入溴的四氯化碳溶液中,观察到的现象是 ;其反应方程式为 。
此外,乙烯能用来生产环氧乙烷,生产工艺主要有两种:
工艺一:
工艺二: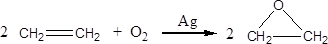
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,因此,在实际生产中,应采用(填“工艺一”或“工艺二”)更环保、更经济。
(4分)下列实验操作或对实验事实的描述中正确的说法有。
①分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
②除去甲烷中混有的少量乙烯,可以让混合物通过盛有酸性KMnO4溶液的洗气装置
③实验室用二氧化锰和稀盐酸制备氯气
④只用溴水就可将苯、四氯化碳、乙醇、己烯四种液体区别开来
⑤用分液法分离苯和硝基苯的混合物
实验室以含有Mg2+、Cl—、Br—、SO42—等离子的卤水为主要原料制备Mg和Br2,流程如下: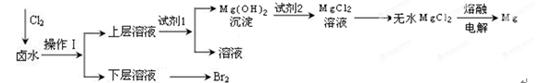
(1)操作Ⅰ使用的试剂是;所用主要仪器的名称是。
(2)为了使Mg2+转化为沉淀,试剂1可以选用;加入试剂1后,能够分离得到Mg(OH)2沉淀的方法是。
(3)试剂2可以选用。
(4)请写出由无水MgCl2生成Mg的化学反应方程式。
(8分)碘在科研与生活中有重要的应用。某兴趣小组用0.50mol·L-1KI 、0.2%淀粉溶液、0.20mol·L-1K2S2O8、0.10mol·L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。已知S2O82—+2I—=2SO42—+I2(慢) I2 +2S2O32—=2I—+S4O62—(快)
(1)向KI 、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中(写离子符号)耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32—与S2O82—初始的物质的量需满足的关系为n(S2O32—)︰n(S2O82—)。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验 序号 |
体积/mL |
||||
| K2S2O8溶液 |
水 |
KI溶液 |
Na2S2O3溶液 |
淀粉溶液 |
|
| ① |
10.0 |
0.0 |
4.0 |
4.0 |
2.0 |
| ② |
9.0 |
1.0 |
4.0 |
4.0 |
2.0 |
| ③ |
8.0 |
VX |
4.0 |
4.0 |
2.0 |
表中VX=mL,理由是。