下列物质:①水晶 ②干冰 ③氨气 ④白磷 ⑤氩 ⑥氯化钠
⑦铁 ⑧晶体硅 ⑨过氧化钠 ⑩H2O 其中:
(1) 将①②④⑥⑧⑩按照熔沸点由高到低的顺序排列 (填序号)
(2)含有极性键的非极性分子的电子式是
(3) 晶体⑥中1个阳离子周围有 个阴离子;熔化时只破坏共价键的晶体是 (填序号)
(4)1 mol金刚石、水晶和白磷中含有共价键的数目之比为
(5)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为 。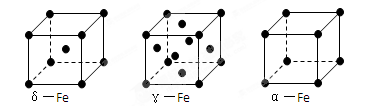
如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题:
(1)打开K2,闭合K1,B为_______极,A的电极反应为_____,最终可观察到的现象是。
(2)打开K1,闭合K2,E为_______极,检验F极产生气体的方法是。该装置中发生反应的化学方程式为_________。
(3)若往U型管中滴加酚酞,进行(1)、(2)操作时,极周围能变红(填A、B、E、或F)。
(4)若电源选用燃料电池,结构如下图,以熔融碳酸盐为电解质(非水溶济,能够传导CO32-),电池工作时电解质组成保持稳定,通入甲烷的电极为________极,请写出正极反应的方程式,若在标况下消耗11.2L的甲烷,电解NaCl溶液产生的H2的物质的量为mol(假设燃料电池能量转化率为75%)。
根据铜锌原电池示意图,回答下列问题:
(1)锌为极,电极反应式为;铜为极,电极反应为,原电池总离子反应式是。
(2)若以该电池作为电源,以石墨碳棒为电极电解CuCl2溶液,在电池的工作过程中,Zn极质量变化了3.25g,则Cu极质量(填“增加”、“不变”或“减少”);电子从电池的锌极沿导线流向电解池的(填“阴极”或“阳极”,下同);在电解池中Cu2+向移动,在该电极上析出铜的质量为g。
人们已经研制出以丙烷为燃料的新型燃料电池,电解质为熔融碳酸盐,电池总反应方程式为:C3H8+5O2=3CO2+4H2O。
(1)已知:2C3H8(g)+7O2(g)=6CO(g)+8H2O(l)
C(s)+O2(g)=CO2(g)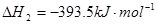
2C(s)+O2(g)=2CO(g)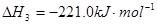
则反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(1)的△H___________________。.
(2)该电池的正极通入O2和CO2,负极通入丙烷,则正极的电极反应式为_________________,电池工作时CO32—移向_____________极。
(3)用该电池电解1L 1 mol·L—1的AgNO3溶液,此电解池反应的化学方程式为______________________;当该电池消耗0.005molC3H8时,所得溶液的pH为__________(溶液体积变化忽略不计)
某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为_________,2s内用A的浓度变化和用B的浓度变化表示的平均反应速率分别为_________、_________。 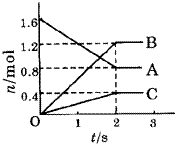
A、B、C三种物质的物质的量随时间变化的关系图
A、B、C、D都是由短周期元素组成的常见物质,其中A、B、C均含同一种元素,在一定条件下相互转化如下图所示(部分产物已略去)。
请按要求回答下列问题:
(1)若B、C 为氧化物,C能够与水反应生成一种强酸E。
①当B为无色易溶于水的刺激性气体时,写出B转化为C的化学方程式:;
②当B为无色不溶于水的气体时, F由A与E化合生成。当小心加热F时,可得到一种无色无味的气体G(G和CO2具有相同的原子数目和电子数目)和一种无色无味的液体H,写出F分解生成G和H的化学方程式;
(2)若D为氧化物,A、B、C都是强电解质,C可用于食品发酵、泡沫灭火。写出A与D反应的离子方程式:;
(3)若D为强酸或强碱溶液时都能发生图示转化关系,且A和C在溶液中反应生成白色沉淀B。
当D为强酸时,A→B反应的离子方程式:;
当D为强碱时,B→C反应的离子方程式:。