设NA为阿伏伽德罗常数的数值,则下列说法中正确的是
①2.24L氨气含有NA个电子,②1.4g乙烯与丙烯的混合气体含有NA个碳原子,③精炼铜, 若阳极失去2NA个电子,则阴极增重64g,④标准状况下,22.4L空气含有NA个分子,⑤过氧化钠与水反应,若电子转移4NA,则产生的氧气为32 g,⑥将1L 2mol/L 的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA,⑦在1L 0.1mol/L的碳酸钠溶液中,阴离子总数大于0.1NA
| A.②③④⑦ | B.①③④⑦ | C.②③④⑤⑦ | D.②④⑤⑦ |
在2升的密闭容器中,发生以下反应:2A (气)+B(气)
(气)+B(气) 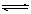 2C气+D(气)。若最初加入的A和B都是4mol,在前10秒钟A的平均反应速度为0.12 mol·L-1·s-1,则10秒钟时,容器中B的物质的量是
2C气+D(气)。若最初加入的A和B都是4mol,在前10秒钟A的平均反应速度为0.12 mol·L-1·s-1,则10秒钟时,容器中B的物质的量是
| A.1.6 mol | B.2.8 mol | C.2.4 mol | D.1.2 mol |
下列说法正确的是
从下列事实,找出不能用勒沙特列原理解释的是
A.在溴水中存在如下平衡: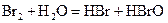 ,当加入NaOH溶液后颜色变浅 ,当加入NaOH溶液后颜色变浅 |
B.对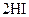   平衡体系增加压强使颜色变深 平衡体系增加压强使颜色变深 |
C.反应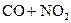  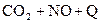 升高温度使平衡向逆方向移动 升高温度使平衡向逆方向移动 |
D.合成氨反应: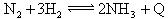 ,为使氨的产率提高,理论上应采取低温高压的措施 ,为使氨的产率提高,理论上应采取低温高压的措施 |
强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ·mol-1。分别向1L 0.5mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是
| A.△H1>△H2>△H3 | B.△H1<△H2<△H3 |
| C.△H1>△H2=△H3 | D.△H1=△H2<△H3 |
有mA(g)+nB(g)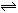 pC(g)+qD(g)反应,经10 min达到平衡,结果A的浓度减少了
pC(g)+qD(g)反应,经10 min达到平衡,结果A的浓度减少了 ,B的浓度减少了
,B的浓度减少了 ,C的浓度增加了
,C的浓度增加了 ,然后增大容器容积, A、 B、C的体积分数不变,则m∶n∶p∶q为( )
,然后增大容器容积, A、 B、C的体积分数不变,则m∶n∶p∶q为( )
A.1∶3∶2∶2 B.2∶3∶3∶2 C.1∶3∶2∶1 D.3∶1∶2∶2