为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如下表:
| |
第I组 |
第Ⅱ组 |
第Ⅲ组 |
| 稀硫酸的质量/g |
50 |
100 |
150 |
| 溶解固体的质量/g |
10.0 |
16.0 |
16.0 |
根据实验及有关数据进行分析与计算:
(1)20g样品中含氧化铜的质量为______g,样品中氧化铜的质量分数为________。
(2)计算所用的稀硫酸溶质的质量分数是多少?(写出计算过程)
(3)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10%NaOH溶液的质量与生成沉淀质量变化关系的曲线图(见答题卡)。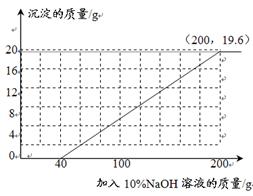
有①Cu-Zn②Cu-Ag两种貌似黄金的合金,它们都有其特殊的用途,但一些骗子常用它们做成饰品冒充真黄金欺骗消费者。对此,化学科学有责任加以揭露。
(1)现有上述两种合金制成的假黄金饰品各一件,小明同学只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是合金(填写代号);若要证明另一种饰品也是假黄金,可选用一种盐溶液来验证,这种盐可以是(写一种盐的名称或化学式);
(2)取与上述用稀盐酸鉴别出的同种合金10g,放入烧杯中,再向其中加入93.7g某稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为103.5g。
①上述过程中变化的质量10g+93.7g-103.5g=0.2g是(填物质的名称或化学式)的质量;
②10g该合金中铜的质量是多少?已知反应后的溶液中溶质全部溶解,求该溶液中溶质的质量分数是多少?
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂说明书的部分信息如图1所示。现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像如下。请根据有关信息回答问题。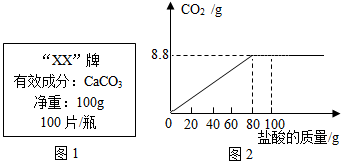
| 第1次 |
第3次 |
第4次 |
|
| 加入盐酸的质量(g) |
20 |
20 |
20 |
| 剩余固体的质量(g) |
35 |
a |
20 |
(1)人体缺钙易出现的疾病是,这时除在医生指导下服用保健药剂外,日常生活中要多摄入等食物。
(2)该品牌补钙药剂中CaCO3的质量分数是,a的数值为。
(3)求5次盐酸加入后所得氯化钙的质量(写出计算过程,4分)。
(6分)某学校化学兴趣小组的同学想测定赤铁矿中氧化铁的含量,做了如下实验:首先称取100 g该赤铁矿样品放入烧杯中,然后将500g的稀盐酸分5次加入烧杯内(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下:
| 第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
|
| 稀盐酸的质量 |
100g |
100g |
100g |
100g |
100g |
| 溶液的质量 |
116.0g |
X |
348.0g |
464.0g |
575.0g |
请回答下列问题:
(1)该小组要用质量分数为36.5%浓盐酸配制所需的500g的稀盐酸,则需浓盐酸的质量为_____
(2)写出实验中发生反应的化学方程式 ____________________
(3)列出求解生成氯化铁总质量的比例式 ____________________
(4)将第二次反应后所得溶液蒸发掉32g水(未达到饱和),则所得溶液的溶质质量分数是________
(5)某工厂要想制得420t含杂质3%的生铁,需要这种赤铁矿的质量为 ___________
(5分)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁。现有废硫酸49 t(H2SO4的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?(答卷纸上写清计算过程)
“黄铜”是铜、锌合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下:(烧杯质量均为56g)
| 甲 |
乙 |
丙 |
|
| 烧杯+稀盐酸质量 |
139g |
129g |
129g |
| 加入黄铜样品质量 |
20g |
24g |
20g |
| 充分反应后,烧杯+剩余物质质量 |
158.8g |
152.8g |
148.8g |
请回答下列问题:
(1)同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是。
(2)计算黄铜样品中锌的质量分数。