现有A、B、C、D、E、F六种短周期元素,A、E处于同一主族且E是短周期元素中原子半径最大的元素(不含稀有气体)。已知C的原子序数等于A、B的原子序数之和;D的原子序数等于A、C的原子序数之和。人类已知的化合物中,有一类化合物的种类已超过三千万,这类化合物中一般都含有A、B两种元素。F是一种生活中常用的金属。根据以上信息,回答下列问题:
(1) 写出元素B在周期表中的位置_____________。
(2) 写出F的单质与E的最高价氧化物对应水化物反应的化学方程式______________。
(3) 比较C、D气态氢化物的稳定性______>_______(填化学式);比较D、E、F原子半径的大小______>________>_______(填元素符号)。
(4) 在A、B、D三种元素中选择两种或三种元素组成两种可以发生反应的阴离子,请写出该反应的离子方程式________________________________________。
(一)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)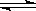 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将 。(填“增大”或“减小”、“不变”)
②下表为反应在T1温度下的部分实验数据:
| t/s |
0 |
500 |
1000 |
| c(N2O5)/mol·L-1 |
5.00 |
3.52 |
2.48 |
则500s内N2O5的分解速率为 。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1。
(二)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g)K1∆H < 0(I)
NaNO3(s)+ClNO(g)K1∆H < 0(I)
2NO(g)+Cl2(g) 2ClNO(g) K2∆H < 0(II)
2ClNO(g) K2∆H < 0(II)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)=
mol,NO的转化率а1= 。其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率а2 а1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”。
(三)已知C(s)+H2O(g)=CO(g)+H2(g)ΔH=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
(一)如图所示,甲、乙是电化学实验装置,请回答下列问题: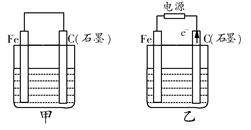
(1)若甲、乙两个烧杯中均盛放饱和NaCl溶液。
①甲中石墨棒上的电极反应式是___________________
②乙中总反应的离子方程式为___________
③若乙中含0.10 mol·L-1NaCl溶液400mL,当阳极产生气体为560mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计),转移电子的个数为
(二)(1)与MnO2—Zn电池类似,K2FeO4—Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为
(2)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态K2CO3为电解质。写出该燃料电池负极的电极反应式:
(三)已知:N2(g)+O2(g)===2NO(g) ΔH=+180.5 kJ/mol;
2C(s)+O2(g)===2CO(g)ΔH=-221.0 kJ/mol;
C(s)+O2(g)===CO2(g)ΔH=-393.5 kJ/mol。
尾气转化的反应之一为NO和CO生成N2和CO2,则该反应的热化学方程式为:
现用18.4 mol·L-1的浓硫酸来配制450mL 0.2 mol·L-1的稀硫酸,可供选择的仪器有:
①玻璃棒 ②烧杯 ③胶头滴管 ④量筒 ⑤托盘天平
(1)上述仪器在配制过程中不需要用到的是__________________(填序号)除上述仪器外,尚缺最重要的仪器是
(2)计算所需浓硫酸的体积为___________mL。(精确到一位小数)
(3)实验中用到玻璃棒,其作用分别是:___________、__________。
(4)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却。
其正确的操作顺序为:②→①→③→_________→_________→_________→_________→④(填序号)
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有____________(填序号)
①定容时,仰视刻度线。
②未冷却至室温就转移到容量瓶中。
③容量瓶中含有少量蒸馏水。
④未洗涤稀释浓硫酸时用过的烧杯和玻璃棒。
⑤定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线。
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,可证明滤液中含Na+,不含K+。
由上述现象推断:
(1)该混合物中一定含有 ;一定不含有 ,可能含有 。
(2)如要检验可能含有的物质是否存在,将如何操作
从氢气、氧气、水、一氧化碳、氧化铜中任意挑选作为反应物,按下列要求写出化学方程式:
①既属于化合反应,又属于氧化还原反应:
②属于氧化还原反应,但不属于置换、化合、分解、复分解反应: