巳知某溶液中存在较多的H+、SO42—、NO3—,则该溶液中还可能大量存在的离子组是( )
| A.Al3+、CH3COO—、Cl— | B.Mg2+、Ba2+、Br— |
| C.Mg2+、Cl—、I— | D.Na+、NH4+、Cl— |
沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态水时放出445 kJ的热量,则下列热化学方程式中正确的是
| A.2CH4(g)+4O2(g)==2CO2(g)+4H2O(1)△H=" +1780" kJ/mol |
| B.CH4(g)+2O2(g)==CO2(g)+2H2O(l)△H=" +890" kJ/mol |
| C.CH4(g)+2O2(g)==CO2(g)+2H2O(1)△H= —890 kJ/mol |
D.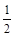 CH4(g)+O2(g)== CH4(g)+O2(g)==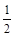 CO2(g)+H2O(1)△H= —890 kJ/mol CO2(g)+H2O(1)△H= —890 kJ/mol |
下列说法正确的是
| A.过渡元素均为金属元素 |
| B.IA族统称为碱金属,最外层有两个电子的原子一定在IIA 族 |
| C.含离子键的晶体一定是离子晶体,含共价键的晶体一定是分子晶体 |
| D.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
下图所示的实验操作,能达到相应目的的是
下列离子方程式正确的是
| A.向稀硝酸中加入铜片:Cu+4H++2NO3- = Cu2++2NO2↑+2H2O |
| B.AlCl3溶液中加入足量的氨水:Al3+ +3OH- = Al(OH)3↓ |
| C.NH4HCO3溶液中加入足量的NaOH溶液:NH4++OH- = NH3↑+ H2O |
| D.向稀硝酸中加入氧化铁:Fe2O3 + 6H+ = 2Fe3+ +3H2O |
如右图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,
立即用另一表面皿扣在上面。下列对实验现象所做的解释正确的是
| A.浓盐酸附近产生白烟:NH3与HCl气体反应产生了NH4C1固体 |
| B.浓硫酸附近无明显现象:NH3与浓硫酸不发生反应 |
| C.氯化物溶液变浑浊:该溶液一定是A1Cl3溶液 |
| D.湿润的红色石蕊试纸变蓝:NH3的水溶液显碱性 |