有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl—、SO42—、HCO3—、MnO4—中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )
| A.肯定有Al3+、Mg2+、HCO3— | B.肯定有A13+、Mg2+、SO42— |
| C.肯定没有HCO3—、MnO4—、NH4+、K+ | D.不能确定K+、Cl—是否存在 |
某草药中有一种色素,它的结构简式为 ,用它制成的试剂可以检验物质的酸碱性。能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是
,用它制成的试剂可以检验物质的酸碱性。能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是
| A.3 mol、5 mol | B.6 mol、8 mol |
| C.10 mol、8 mol | D.6 mol、10 mol |
历史上最早应用的还原性染料——靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中不正确的是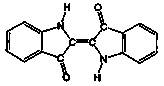
| A.靛蓝由碳、氢、氧、氮四种元素组成 | B.它的分子式是C16H10N2O2 |
| C.该物质是高分子化合物 | D.它是不饱和的有机物 |
将0.2mol两种气态烃组成的混合气完全燃烧后得到6.72升二氧化碳(标准状况下)和7.2克水, 下列关于该混合烃说法正确的是
| A.一定有乙烯 | B.一定有甲烷 |
| C.一定没有甲烷 | D.可能有乙炔 |
已知酸性大小:羧酸>碳酸>酚。下列含溴化合物中的溴原子,在适当条件下都能被羟基(-OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是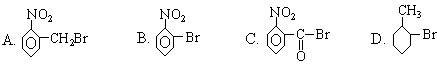
实验室为除去苯中含有的少量苯酚,通常采用的方法是
| A.加热蒸馏,用分馏法分离 | B.加乙醇,用分液漏斗分离 |
| C.加氢氧化钠溶液,用分液漏斗分离 | D.加浓溴水,用过滤法分离 |