已知反应mA(g)+nB(g) qD(g)的△H<0,m+n>q,在一个体积固定的密闭容器中反应达到平衡时,下列说法正确的是
qD(g)的△H<0,m+n>q,在一个体积固定的密闭容器中反应达到平衡时,下列说法正确的是
| A.增加A的质量,B的转化率降低 | B.降低温度,混合气体的平均相对分子质量变小 |
| C.通入稀有气体压强增大,平衡向正反应方向移动 | D.B的正反应速率是A的逆反应速率的n/m |
把0.1mol铝投入到。 100mL3mol/L的.NaOH溶液中充分反应后,再滴人lmol/L的H2SO4120mL,其结果( )
100mL3mol/L的.NaOH溶液中充分反应后,再滴人lmol/L的H2SO4120mL,其结果( )
| A.溶液的pH<7 | B.得到澄清透明溶液 |
| C.有沉淀生成 | D.先有白色沉淀生成,后逐渐溶解 |
250C时,重水(D2O)的离子积为1.6×10-15也可用pH值一样的定义来规定其酸碱度:pD==-lgCD+,下列叙述正确的是( )
①中性D2O的pD=7
②在1LD2O中,溶解0.01molDCl,其pD值为1
③1L0.1mol/L的NaOD的重水溶液,pD=12
④在100mL0 .25rnoL/LDCl的重水溶液中,加入50mL0. 2mo1./L NaOD的重水溶液,反应后溶液的pD=1
⑤温度升高,CD+×COD-的值会升高
| A.②③ | B.③④ | C.①② | D.④⑤ |
对于可逆反应Na2(g)+3H2(g)=2NH3(g) 2NH3(g;)△H<0,以下各影响因素改变和示意图相符合的是( )
2NH3(g;)△H<0,以下各影响因素改变和示意图相符合的是( )
| A |
B |
C |
D |
|
| 影响因素 |
压强对反应的影响(P2>P1) |
温度对反应的影响 |
平衡体系增加NH3对反应的影响 |
催化剂对方应的影响 |
| 图示 |
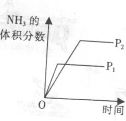 [ [ |
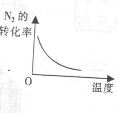 |
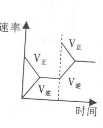 |
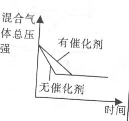 |
下列各组混合物的分离或提纯方法不正确的是( )
| A.除去溴化钠溶液中含有的碘化钠:加入氯水充分振荡后,再加四氯化碳,萃取分液 |
| B.用结晶法提纯NaC和KNO3的混合物中的KNO3 |
| C.用蒸馏法分离汽油和柴油混合物 |
| D.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
下列离子方程式书写正确的是( )
| A.碳酸氢钙溶液加到醋酸中:Ca(HCO3)2+2CH3COOH===CA2++2CH3COO-+2CO2á+2H2O |
| B.FeI2溶液中通人少量的Cl2:2Fe2++CO2====2Fe3++2CL- |
C.饱和Fecl3溶液滴入沸水中Fe3++3H2O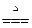 Fe(OH)3(胶体)+3H+ Fe(OH)3(胶体)+3H+ |
| D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-====BaCO3â +2H2O+CO32- |