A、B、C、D为单质,其余物质为化合物。A为银白色金属,D为黑色固体非金属,X在常温下是无色液体,B、C、J在常温下为气体。分别用铂丝蘸取少许E、F、H、I溶液,在无色火焰上灼烧,火焰呈黄色。将J通入澄清石灰水,石灰水先变浑浊,继续通J一段时间,石灰水又变澄清。物质间有如下图转化关系。(图中省略部分反应物和生成物)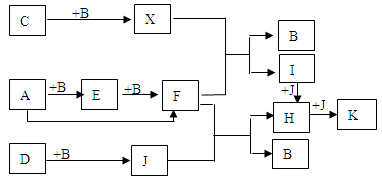
(1)请写出下列物质的化学式:
A:B:X:J:
(2)写出下列变化中的化学反应方程式,是离子反应的,写离子反应方程式。
①A→F;
②X+F→B+I
(3)F在生产和生活中具有重要作用,写出F的一种用途。
(4)如果I溶液中混有H,要除去H应加适量___溶液(填化学式),离子方程式为 。
为探索工业含铝、铁、铜合金废料的再利用,某同学实验设计的回收利用方案如下: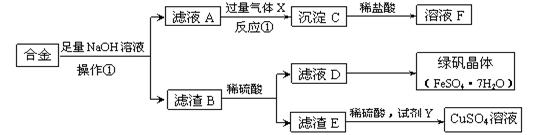
(1)操作①的名称是 , 滤渣B含有(填化学式)。
(2)反应①的离子方程式是。
(3)若要从滤液D得到绿矾晶体,必须进行的实验操作步骤:、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有(填序号)。
A.漏斗B.坩埚C.烧杯D.玻璃棒
(4)试剂Y应该是一种(填“氧化剂”或“还原剂”),它不可能是(填序号)。
A.H2O2B.H2C.O2D.Fe
(原创)(1)除去碳酸钠固体中少量碳酸氢钠的方法是,化学方程式为 。
(2)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
Fe(OH)3 +ClO-+OH-===FeO42-+Cl-+()
(3)某溶液中可能大量含有Mg2+、Cu2+、Al3+、Cl-、OH-、CO32-。当加入氢氧化钠溶液时,生成白色沉淀的
物质的量与加入氢氧化钠的物质的量关系如图所示。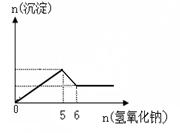
则溶液中大量含有的离子有______________________,各离子的物质的量浓度之比为____(与前面的离子顺序相对应)。
一同学将一小块金属钠露置于空气中,观察到下列现象:银白色 变灰暗
变灰暗 变白色
变白色 出现液滴
出现液滴 白色固体,下列说法正确的是
白色固体,下列说法正确的是
| A.①发生了氧化还原反应 |
| B.②变白色是因为生成了碳酸钠 |
| C.③是碳酸钠吸收空气中的水蒸气形成了溶液 |
| D.④只发生物理变化 |
(11分)如下图,A、B是中学化学里常用的物质,已知A是化合物,B是单质;E溶液中滴入KSCN溶液呈红色。试回答: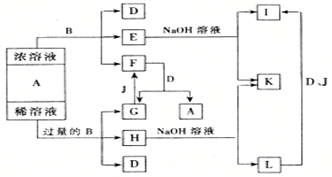
(1)B和A的浓溶液反应的条件是,简述常温下不易反应的原因。
(2)写出F和G相互转化的化学方程式
F→G。
G→F。
(3)简述L转化为I的现象,该反应的化学方程式为。