三苯甲醇(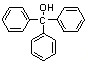 )是重要的有机合成中间体,实验室中合成三苯甲醇时采用图2所示的装置,其合成流程如图1所示。
)是重要的有机合成中间体,实验室中合成三苯甲醇时采用图2所示的装置,其合成流程如图1所示。
图1
已知:(1)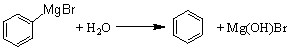 (碱式溴化镁);
(碱式溴化镁);
(2)相关物质的物理性质如下:
| 物质 |
熔点 |
沸点 |
溶解性 |
| 三苯甲醇 |
164.2℃ |
380℃ |
不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 |
-116.3℃ |
34.6℃ |
微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 |
-30.7°C |
156.2°C |
不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 |
-34.6°C |
212.6°C |
不溶于水 |
| Mg(OH)Br |
常温下为固体 |
能溶于水,不溶于醇、醚等有机溶剂 |
请回答以下问题:
(1)写出装置图中玻璃仪器的名称:A ,导管B的作用 ;
(2)制取格氏试剂时要保持微沸,可以采用水浴加热,优点是 ,微沸回流时冷凝管中水流的方向是
(填“X→Y”或“Y→X”),装有无水CaCl2的仪器A的作用是 ;
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写空白:


图2 图3
(4)抽滤时所用装置如图3所示,该装置存在的错误有 ,抽滤完毕或中途停止抽滤时的操作方法:应先 ,然后 ;
(5)洗涤液最好选用 ,检验产品已经洗涤干净的操作为 。
(A)水(B)乙醚 (C)乙醇 (D)苯
某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验。
(1)根据图A写出实验室制取氨气的化学方程式_________________________;
如何检验氨气已经收集满。
(2)甲同学用干燥的圆底烧瓶收集一瓶氨气,根据图B进行实验,观察到的实验现象是______________________________________________。根据实验现象说明氨气具有的性质是_____________________________________。
某校化学兴趣小组为研究Cl2的性质,设计如下图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式是。
(2)装置Ⅱ的作用是。
(3)实验过程中,装置IV中的实验现象为___________________________________;发生反应的化学方程式为。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置与之间添加下图中的装置(填序号),该装置的作用是______________________。
(5)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式。
Na2S2O3俗称大苏打(海波)是重要的化工原料。用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3。已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g。常温下,从溶液中析出的晶体是Na2S2O3·5H2O。
现实验室欲制取Na2S2O3·5H2O晶体(Na2S2O3·5H2O的分子量为248)
步骤如下:
①称取12.6g Na2SO3于烧杯中,溶于80.0mL水。
②另取4.0g硫粉,用少许乙醇润湿后,加到上述溶液中。
③(如图所示,部分装置略去),水浴加热,微沸,反应约1小时后过滤。
④滤液在经过、后析出Na2S2O3·5H2O晶体。
⑤进行减压过滤并干燥。
(1)仪器B的名称是________。其作用是_______________。加入的硫粉用乙醇润湿的目的是。
(2)步骤④应采取的操作是、。
(3)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机杂质。如果滤液中该杂质的含量不很低,其检测的方法是:。
(4)为了测产品的纯度,称取7.40g 产品,配制成250mL溶液,用移液管移取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol/L 的碘水,用(填“酸式”或“碱式”)滴定管来滴定(2S2O32-+ I2= S4O62-+ 2I-),滴定结果如下:
| 滴定次数 |
滴定前读数(mL) |
滴定滴定后读数(mL) |
| 第一次 |
0.30 |
31.12 |
| 第二次 |
0.36 |
31.56 |
| 第三次 |
1.10 |
31.88 |
则所得产品的纯度为,你认为影响纯度的主要原因是(不考虑操作引起误差)。
为测定某混合物中各组分的质量分数(已知该混合物含NaCl、Na2CO3•10H2O和NaHCO3),设计如下:
实验:
(1)加热前通入空气的目的是 ______________,操作方法为_______________________________。
(2)装置C中盛放的试剂可以是___________(填序号)。
a.碱石灰b.无水CaCl2c.P2O5d.固体NaOH
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将________(填“偏高”、“偏低”或“无影响”,下同);若撤去E装置,则测得Na2CO3•10H2O的含量。
(4)若样品质量为 w g,反应后C、D增加的质量分别为 m1 g、m2 g,由此可知混合物中NaHCO3质量分数为_____________________(用含w、m1、m2的代数式表示)
某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题: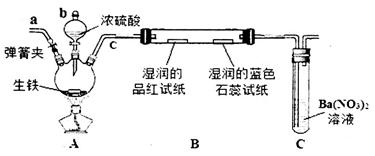
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为_____________:实验过程中,装置B中观察的现象是_______________;装置C中有白色沉淀生成,该沉淀是______________(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:_____________________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为__________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是________________________________。
(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是___________________(用离子方程式表示)。