某溶液中可能存在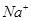 、
、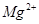 、
、 、
、 、
、 、
、 、
、 等七种离子中的几种。现取该溶液进行实验,得到如下实验现象: ①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生; ②向所得橙色溶液中加入足量
等七种离子中的几种。现取该溶液进行实验,得到如下实验现象: ①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生; ②向所得橙色溶液中加入足量 溶液,无沉淀生成; ③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
溶液,无沉淀生成; ③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断,该溶液中肯定不存在的离子是
A. 、 、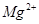 、 、 、 、 |
B.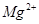 、 、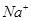 、 、 、 、 |
C. 、 、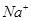 、 、 、 、 |
D. 、 、 、 、 、 、 |
在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的有
| A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I- |
| B.所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ |
| C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D.pH为1的溶液:Cu2+、Na+、Mg2+、NO3- |
在一密闭容器中有如下反应:L(s)+aG(g)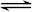 bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断
bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断
| A.正反应为放热反应 |
| B.化学方程式中的计量数a>b |
| C.G的转化率随温度升高而减小 |
| D.增大压强,容器内气体质量不变 |
用标准的KOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是
| A.配制标准溶液的固体KOH中混有NaOH杂质 |
| B.滴定终点读数时,仰视滴定管的刻度,其他操作正确 |
| C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗 |
| D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液 |
将标况下的2.24LCO2通入150mL 1mol/LNaOH溶液中,下列说法正确的是
| A.c(Na+)等于c(CO32-)与c(HCO3-)之和 | B.c(HCO3-) 等于c(CO32-) |
| C.c(HCO3-) 略大于c(CO32-) | D.c(HCO3-) 略小于c(CO32-) |
下列说法中正确的是
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 |
B.AgCl悬浊液中存在平衡:AgCl(s) 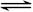 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 |
| C.为减小洗涤过程中固体的损失,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀 |
| D.硬水中含有较多的Ca2+、Mg2+、HCO3-、SO42-,加热煮沸可以完全除去其中的 Ca2+、Mg2+ |