反应mA(s)+nB(g) pC(g) ΔH<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
pC(g) ΔH<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )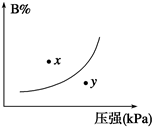
①m+n>p ②x点表示的正反应速率大于逆反应速率 ③x点比y点时的反应速率慢 ④n>p ⑤若升高温度,该反应的平衡常数增大
| A.①②⑤ | B.只有②④ | C.只有②③ | D.①③⑤ |
一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g) +2H2O(g)△H1="-" 574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=—1160kJ·mol-1
下列选项正确的是
| A.CH4 (g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=" -" 867kJ·mol-1 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)的反应热为△H3, 则△H3>△H1 |
| C.若用0.2molCH4还原NO2至N2,则反应中放出的热量一定为173.4kJ |
| D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6mol |
NH3中氢原子可被锂原子替代。亚氨基锂(Li2NH)是一种良好的固体储氢材料,其储氢原理可表示为Li2NH+H2→LiNH2+LiH。下列有关说法正确的是
| A.Li2NH中N的化合价为-1 |
| B.此法储氢和钢瓶储氢的原理相同 |
| C.LiH中的阳离子半径大于阴离子半径 |
| D.该反应中H2既是氧化剂又是还原剂 |
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
| A.电子通过外电路从b极流向a极 |
| B.H+由a极通过固体酸电解质传递到b极 |
| C.b极上的电极反应式为:O2+2H2O+4e-=4OH- |
| D.每转移0.1 mol电子,消耗1.12 L的H2 |
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1mol的混合溶液中加入0.1mol铁粉,充分搅拌后铁完全反应,溶液中不存在Fe3+,同时析出0.1molAg。则下列结论中不正确的是
A.反应后溶液中Cu2+与 Fe2+的物质的量之比为1:2 Fe2+的物质的量之比为1:2 |
B.氧化性:Ag+>Fe 3+>Cu2+>Zn2+ 3+>Cu2+>Zn2+ |
| C.含Fe3+的溶液可腐蚀铜板 |
| D.1molFe可还原1molFe3+ |
下列离子方程式中,正确的是
| A.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH- + O2↑ |
| B.向稀硝酸中加入少量铁粉:3Fe + 8H+ + 2NO3-= 3Fe2+ + 2NO↑ + 4H2O |
| C.氯化镁溶液与氨水反应:Mg2+ + 2OH-=Mg(OH)2↓ |
| D.向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42—+2Ba2++4OH—=2BaSO4↓+AlO2—+2H2O |