微生物燃料电池因具有原料广泛、操作条件温和、清洁高效和资源利用率高、无污染等特点而被人们所重视.以用葡萄糖作底物的燃料电池为例,其正负极反应式如下:
正极反应:6O2+24H++24e-12H2O
负极反应:C6H12O6+6H2O-24e-6CO2↑+24H+
则有关该电池的下列说法正确的是
| A.该电池的工作环境是高温条件 |
| B.作为负极的葡萄糖(C6H12O6)在变化中失去电子,被还原 |
| C.该电池的电解质溶液是强酸性溶液,如浓硫酸或硝酸等 |
| D.该电池的总反应为C6H12O6+6O2===6CO2+6H2O |
在甲酸的下列性质中,可以证明它是弱电解质的是()
| A.甲酸能与水以任意比例互溶 |
| B.1mol/L的甲酸溶液中c(H+)约为1×10-2 mol/L |
| C.1mol/L的甲酸溶液10mL恰好与10mL1mol/L的NaOH溶液完全反应 |
| D.在相同条件下,甲酸溶液的导电性比盐酸弱 |
在一定温度下,可逆反应A(g)+3B(g)  2C(g)达到平衡的标志是()
2C(g)达到平衡的标志是()
| A.A的生成速率与C分解的速率相等 |
| B.单位时间生成nmolA,同时生成3nmolB |
| C.单位时间生成nmolA,同时生成2nmolC |
| D.单位时间生成B的速率与生成C的速率相等 |
下列有利于反应自发进行的是()
①反应吸热②反应放热③反应后熵增加④反应后熵减小
| A.①③ | B.②③ | C.②④ | D.①④ |
反应A(g)+3B(g) 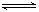 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是()
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是()
A.υ(D)="0.4" mol / (L·s) B.υ(C)="0.5" mol / (L·s)
C.υ(B)="0.6" mol / (L·s)D.υ(A)="0.15" mol / (L·s)
一支25mL滴定管,内盛溶液液面在15.00mL刻度处,当将滴定管内液体全部排出时,所得液体的体积是()
| A.10.00mL | B.15.00mL | C.小于10.00mL | D.大于10.00mL |