工业上处理含Cr2O72—的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准.试回答:
(1)电解时的电极反应:阳极________________,阴极__________________________.
(2)Cr2O72—转变成Cr3+的离子反应方程式:_____________________.
(3)电解过程Cr(OH)3、Fe(OH)3沉淀是怎么产生的?
______________________________________.
(4)能否用Cu电极来代替Fe电极?________(填“能”或“不能”),简述理由______________________.
、
、
、
、
五种元素分属三个短周期,且原子序数依次增大。
、
同主族,可形成离子化合物
;
、
同主族,可形成
、
两种分子。
请回答下列问题:
⑴
在元素周期表中的位置为。
⑵ 上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式),非金属气态氢化物还原性最强的是(写化学式)。
⑶
、
的单质或两元素之间形成的化合物可作水消毒剂的有(写出其中两种物质的化学式)。
⑷
的燃烧热
,写出
燃烧反应的热化学方程式:
⑸
的电子式为;
与水反应放出气体的化学方程式为。
⑹ 熔融状态下,
的单质和
能组成可充电电池(装置示意图如下),反应原理为:
2
+
 ;放电时,电池的正极反应式为:充电时,(写物质名称)电极接电源的负极;该电池的电解质为。
;放电时,电池的正极反应式为:充电时,(写物质名称)电极接电源的负极;该电池的电解质为。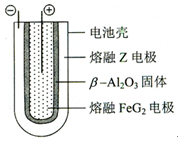
是一种可降解的聚酯类高分子材料,可由马来酸酐等原料经下列路线合成:
(已知: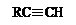 +
+ 

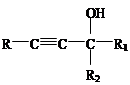 )
)
(1)
的反应类型是;
的结构简式是。
(2)
中含有的官能团名称是;
的名称(系统命名)是。
(3)半方酸是马来酸酐的同分异构体,分子中含1个环(四元碳环)和1个羟基,但不含
键。半方酸的结构简式是。
(4)由
和
合成
的化学方程式是。
(5)下列关于
的说法正确的是。
a.能使酸性
溶液或溴的
溶液褪色
b.能与
反应,但不与
反应
c.能与新制
反应
d.1
完全燃烧消耗5
、
、
、
是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 |
相关信息 |
|
的基态原子
层电子数是
层电子数的2倍 |
|
| 的基态原子最外层电子排布式为: | |
|
存在质量数为23,中子数为12的核素 |
|
|
有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
⑴
位于元素周期表第周期第族,其基态原子最外层有个电子。
⑵
的电负性比
的(填"大"或"小");
和
的气态氢化物中,较稳定的是(写化学式)
⑶写出
与
反应的化学方程式,并标出电子转移的方向和数目:。
⑷在
原子与氢原子形成的多种分子中,有些分子的核磁共振氢谱显示有两种氢,写出其中一种分子的名称:。氢元素、
、
的原子也可共同形成多种分子和某种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式:。
[化学一有机化学基础]
对二甲苯(英文名称
,缩写为
)是化学工业的重要原料。
(1)写出PX的结构简式。
(2)PX 可发生的反应有、(填反应类型)。
(3)增塑剂(DEHP)存在如下图所示的转化关系,其中
是PX的一种同分异构体。
①
的苯环上存在2 种不同化学环境的氢原子,则
的结构简式是。
②
分子所含官能团是(填名称)。
③
分子有1个碳原子连接乙基和正丁基,DEHP的结构简式是
(4)
是
的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物;
.遇
溶液显示特征颜色;
.能与碳酸氢钠溶液反应。
写出
与
溶液反应的化学方程式
(1)元素的第一电离能:
(填">"或"<")。
(2)基态
的核外电子排布式为。
(3)硅烷(
)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是。
(4)硼砂是含结晶水的四硼酸钠,其阴离子
(含
三种元素)的球棍模型如图所示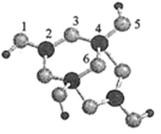
①在
中,硼原子轨道的杂化类型有;配位键存在于原子之间(填原子的数字标号);
=(填数字)。
②硼砂晶体由
、
和
构成,它们之间的作用力有(填序号)。
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键