CO2的摩尔质量是 ;2molCO2的质量是 ;它在标准状况下所占的体积约为 ,所含的分子数目约为 ;所含氧原子的数目约为 。
在25℃时,用石墨电极电解2.0L,2.5 mol/LCuSO4溶液。5 min后,在一个石墨电极上有6.4gCu生成。试回答下列问题:
(1)极发生氧化反应(填阴,阳),电极反应式为。
(2)极发生还原反应(填阴,阳),电极反应式为。
(3)有mol电子发生转移,得到氧气的体积(标准状况)是L,溶液的pH是。反应速率v(Cu2+):v(O2)==
(4)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差g,电解液的pH(填“变小”、“变大”或“不变”)
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
(1)a极是极,b极是极,
电极反应式分别为,。
(2)氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料,往往是某些碳氢化合物,如甲烷(天然气)、汽油等。请写出将图中H2换成CH4时所构成的甲烷燃料电池中a极的电极反应式:。此时电池内总的反应方程式为。
已知难溶于水的盐在水中存在溶解平衡: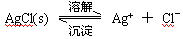
在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 KSP表示:KSP= c(Ag+)·c(Cl-)=1.8·10-10。
若把足量AgCl分别放入① 100 mL蒸馏水,② 100 mL 0.1 mol / L NaCl溶液,③ 100 mL 0.1 mol / L AlCl3溶液,④ 100 mL 0.1 mol / L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是 ______>______>______>______。在0.1 mol / L AlCl3溶液中,Ag+的物质的量浓度最多为_________mol / L。
10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
| pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度(填“大于”或“小于”)NaHCO3。丙同学认为甲、乙的判断都不充分。丙认为:
⑴只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则(填“甲”或“乙”)判断正确。试剂X是。
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
⑵将加热后的溶液冷却到10℃,若溶液的pH(填“高于”、“低于”或“等于”)8.3,则(填“甲”或“乙”)判断正确。
⑶查阅资料,发现NaHCO3的分解温度为150℃,丙断言(填“甲”或“乙”)判断是错误的,理由是。
用标准酸液滴定待测碱液时,下列操作对所测碱液的物质的量浓度有何影响。
A、偏低 B、偏高 C、无影响
请用序号填空
(1)用待测液润洗锥形瓶后再注入所量取的一定体积待测液____________
(2)未用标准液润洗酸式滴定管就直接注入标准酸液_________________
(3)用滴定管尖端未排气泡的碱式滴定管量取待测碱液_________________
(4)滴定前仰视读数、滴定后俯视读数_______________________________
(5)锥形瓶未润洗,且瓶中有少量蒸馏水_____________________________