用下面方法可以制得白色的Fe(OH)2沉淀。
用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入
________________________________________________________________________。
(2)除去蒸馏水中溶解的O2常采用________的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是
________________________________________________________________________。
(本题共12分)某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出)
实验选用细铜丝、98.3% H2SO4、品红溶液、澄清石灰水、CCl4、NaOH溶液等药品,铜丝被卷成螺旋状,一端没入浓H2SO4中,另一端露置在液面上方。
|
以下是该学习小组部分交流记录及后续探究实验的记录

下列有关化学实验的操作或说法中,正确的是(填字母序号)。
| A.过滤、蒸发操作过程中都需要用玻璃棒不断搅拌液体。 |
| B.检验红砖中的氧化铁成分时,向红砖粉末中加入盐酸,放置至充分沉淀后,取上层清液于试管中,滴加KSCN溶液2滴~3滴即可 |
| C.中和滴定实验中,锥形瓶内有少量蒸馏水会造成测定结果偏低。 |
| D.在进行硫酸铜晶体里结晶水含量的测定实验中,称量操作至少要进行4次。 |
E.制备硫酸亚铁晶体时,向稀硫酸中加入废铁屑至有少量气泡发生时,过滤,然后加热蒸干滤液即可得硫酸亚铁晶体。
F.向2mLl0%NaOH溶液中滴入2%CuSO4溶液的4—6滴,振荡后加入乙醛溶液0.5mL,加热至沸腾,则有红色沉淀出现。
某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(1)通过钠在CO2气体中燃烧的实验,你认为燃烧的条件是。
(2)燃烧的本质是。
(3)2010年8月初发生的俄罗斯森林大火有比伦敦市还要大的面积。控制森林火灾是世界性难题。根据燃烧的条件,请你解释为什么设置森林防火隔离带能有效阻止森林火灾的蔓延?。
【提出假设】
假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3。
假设3:白色物质是Na2O和Na2CO3的混合物。
【设计实验方案.验证假设】该小组对燃烧后的白色产物进行如下探究:
| 实验方案 |
实验操作 |
实验现象 |
结论 |
| 方案1 |
取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 |
溶液变成红色 |
白色物质为Na3O |
| 方案2 |
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 |
出现白色沉淀 |
|
| ③静置片刻,取上层清液于试管中,滴加无色酚酞试液 |
无明显现象 |
【思考与交流】
(4)甲同学认为方案1得到的结论不正确,其理由是。
(5)乙同学认为方案2得到的结论正确,白色物质为。
(6)通过方案1和方案2的实验,你认为上述三个假设中,成立。你的理由是。
(7)钠在二氧化碳中燃烧的化学方程式为。
(8)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:。
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4·5H2O及纳米材料G,步骤如下: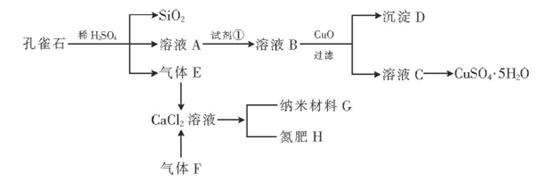
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中,试剂①最佳为(填代号),检验溶液A中Fe3+的最佳试剂为(填代号)。
a. KMnO4b.(NH4)2S c.H2O2 d.KSCN
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为。加入CuO作用是。
(2)由溶液C获得CuSO4·5H2O,需要经过一系列操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是。
(3)制备纳米材料G时,应向CaCl2溶液中先通入(或先加入)(填化学式)。写出该反应的化学方程式。
(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4标准溶液应用(填写仪器名称);取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,终点现象为。
羟基磷灰石(化学式为Ca10(PO4)6(OH)2,简称HA)是一种重要的生物材料。用磷酸与氢氧化钙制备HA的流程如下:
(1)配制石灰乳时,用广泛pH试纸测定溶液的pH值,操作方法是。
(2)步骤②中适宜的加热方法是。
(3)步骤②、③中必须充分搅拌,其目的是
。
(4)步骤④中需将生成的白色胶状沉淀过滤,再用蒸馏水洗涤数次,洗涤的目的是。
(5)实验②中滴入磷酸时,pH随“磷酸的用量与理论量比值”(用K表示)的变化如右图,需要严格控制滴定速率的阶段是。(用K的范围表示)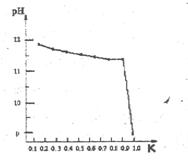
(6)氢氧化钙与磷酸中和生成HA的化学方程式是。